Boilio dėsnis (Boilio–Marioto): apibrėžimas, formulė ir pavyzdys
Sužinokite Boilio–Marioto dėsnį: formulė, aiškinimas ir paprastas pavyzdys – kaip slėgis ir tūris susiję idealiųjų dujų atveju.
Boilio dėsnis (dar vadinamas Marioto dėsniu ir Boilio–Marioto dėsniu) yra dėsnis apie idealiąsias dujas.
Apibrėžimas
Nustatytoje temperatūroje laikomų idealiųjų dujų P (slėgis) ir V (tūris) yra atvirkščiai proporcingi.
Tai reiškia: pastovios masės idealiųjų dujų tūris, esant pastoviai temperatūrai, mažėja, kai didėja jų slėgis, ir atvirkščiai.
Prielaidos
- Temperatūra yra pastovi (izoterminis procesas).
- Dujų masė (molis) yra pastovi — sistema yra uždara, nepristatomos ar neišleidžiamos dujos.
- Dujos elgiasi pagal idealiųjų dujų prielaidas (pakankamai mažas slėgis ir pakankamai aukšta temperatūra).
Formulė
Matematiškai dėsnis reiškiamas kaip atvirkštinė proporcija:
P ∝ 1 V {\displaystyle P\propto {\frac {1}{V}}}
arba
P V = k {\displaystyle PV=k}
čia P – dujų slėgis, V – dujų tūris, o k – pastovi konstanta (priklausanti nuo dujų masės ir temperatūros).
Išvedimas / ryšys su idealiosiomis dujomis
Jei turime dvi būsenas to paties dujų kiekio esant tą pačią temperatūrą, gauname:
P 1 V 1 = k {\displaystyle P_{1}V_{1}=k}
P 2 V 2 = k {\displaystyle P_{2}V_{2}=k}
Nustatę, kad k abiem atvejais ta pati, gauname formulę, kurią dažnai naudojame praktikoje:
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}
Pavyzdžiui, susiejus su idealiųjų dujų įstatymu PV = nRT, jei n (moliai) ir T (temperatūra) yra pastovūs, tuomet PV iš tiesų yra pastovi konstantė k = nRT, todėl Boilio dėsnis yra specialus idealiosios dujų įstatymo atvejis izoterminiam procesui.
Fizinė prasmė
Jei sumažiname tūrio dydį, tuo pačiu tūriu dabar patenka daugiau dujų susidūrimų su sienelėmis per vienetą laiko — tai padidina slėgį. Atvirkščiai, didinant tūrį susidūrimų skaičius mažėja, todėl slėgis mažėja.
Pavyzdys (išsprendimas)
Pavyzdys: Dujų slėgis yra 3 atm, o tūris — 5 litrai. Jei slėgis sumažintas iki 2 atm, koks tūris?
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}
Išreiškiame V2:
V 2 = P 1 V 1 P 2 {\displaystyle V_{2}={\frac {P_{1}V_{1}}{P_{2}}}}
Pakeičiame skaičiavimui:
V 2 = 3 ∗ 5 2 {\displaystyle V_{2}={\frac {3*5}{2}}}
V 2 = 15 2 {\displaystyle V_{2}={\frac {15}{2}}}
V 2 = 7,5 {\displaystyle V_{2}=7,5}
∴ Tūris bus 7,5 litro.
Apribojimai ir taikyba
- Boilio dėsnis taikomas gerai tuo atveju, kai dujos elgiasi arti idealiųjų dujų modelio. Esant labai aukštam slėgiui arba labai žemai temperatūrai, realiosios dujos nukrypsta nuo dėsnio (tada taikomi, pvz., van der Waalso dėsniai ar kiti korekciniai modeliai).
- Dėsnis galioja uždarose sistemose (kai dujų kiekis nepasikeičia). Atidarant sistemą ar keičiant masę, formulė P1V1 = P2V2 nebetinka.
- Praktinis taikymas: pavarų cilindrai, užslėgtų dujų balionai, medicininiai švirkštai, izoterminės procedūros laboratorijose ir kt.
- Dažniausiai naudojamos matavimo vienetų konversijos: 1 atm = 101325 Pa; tūris litrais (L) arba kubiniais metrais (m³).
Istorija
Dėsnis pirmą kartą buvo aprašytas 1662 m. Roberto Boilio. Nepriklausomai nuo jo, panašų dėsniui rezultatą pateikė ir Edme Mariotas (jo darbai apie šią priklausomybę publikuoti XVII a.).
Santrauka: Boilio dėsnis teigia, kad izoterminiu režimu esantis pastovios masės dujų tūris yra atvirkščiai proporcingas jų slėgiui, o tai išreiškiama paprastomis formulėmis PV = k arba P1V1 = P2V2.
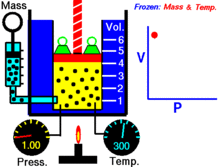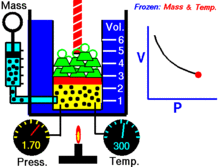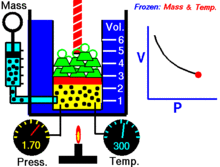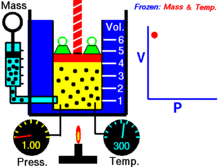
Animacija, rodanti slėgio ir tūrio priklausomybę.Dujų kiekis ir temperatūra yra pastovūs.
Klausimai ir atsakymai
K: Kas yra Boilio dėsnis?
A: Boilio dėsnis (dar vadinamas Marioto dėsniu ir Boilio-Marioto dėsniu) - tai dėsnis apie idealiąsias dujas, teigiantis, kad pastovioje temperatūroje laikomų idealiųjų dujų pastoviam kiekiui slėgis (P) ir tūris (V) yra atvirkščiai proporcingi.
Klausimas: Kaip Boilio dėsnį galime išreikšti matematiškai?
A: Boilio dėsnį matematiškai galime išreikšti taip: P ∝ 1/V arba PV = k, kur P - dujų slėgis, V - dujų tūris, o k - konstanta.
K: Kas atrado šį dėsnį?
A: 1662 m. dėsnį atrado Robertas Boilas, o 1679 m. nepriklausomai nuo jo - Edmas Mariotas.
K: Ką reiškia, kai sakome, kad P ir V yra atvirkščiai proporcingi?
Atsakymas: Tai reiškia, kad vienam iš jų didėjant, kitas proporcingai mažėja - taigi, jei sumažinsite talpyklos, kurioje yra tam tikras dujų kiekis, tūrį, esant tam tikram slėgiui, dėl padidėjusių dalelių susidūrimų, atsirandančių dėl to, kad jos yra mažesnėje erdvėje, slėgis padidės.
Klausimas: Kaip naudojame Boilio dėsnį slėgio arba tūrio pokyčiams apskaičiuoti?
A: Boilio dėsnį galime naudoti slėgio arba tūrio pokyčiams apskaičiuoti naudodami dvi lygtis: P1V1=k ir P2V2=k, kur k išlieka pastovus, o P1/V1 arba P2/V2 keičiasi priklausomai nuo to, ką norite apskaičiuoti.
Klausimas: Ar šį dėsnį galime taikyti ir realioms dujoms?
Atsakymas: Ne - šis dėsnis taikomas tik idealiosioms dujoms, nes tarp jų nėra tarpmolekulinių jėgų.
Ieškoti








