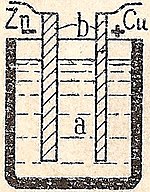
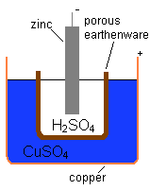
Cheminis elementas cheminę energiją paverčia elektros energija. Dauguma baterijų yra cheminiai elementai: akumuliatoriuje vyksta cheminė reakcija, dėl kurios teka elektros srovė. Šią reakciją lemia medžiagų, vadinamų anodu, katodu ir elektrolytu, savybės — keičiantis jų cheminėms būsenoms, išlaisvėja arba surenkama energija, kurią galima naudoti elektros grandinėje.
Yra du pagrindiniai akumuliatorių tipai - įkraunami ir neįkraunami. Kiekvienas tipas turi savų privalumų ir trūkumų, todėl parinkimas priklauso nuo paskirties (vienkartinis naudojimas, ilgalaikė talpa, galingumas, kaina ir kt.).
Neįkraunamas akumuliatorius elektros energiją tiekia tol, kol jame esančios cheminės medžiagos sunaudojamos. Tuomet jis tampa nebenaudinga ir paprastai išmetamas arba perdirbamas. Tokį sprendimą galima apibūdinti kaip "naudok ir išmesk". Dažniausi neįkraunami tipai: cinko-anglies (anglies-cinko), alkaliniai (mangano dioksido ir cinko) bei kai kurie ličio vienkartiniai elementai — jie pasižymi paprastumu, žema kaina ir stabilia nominalia įtampa (pvz., 1,5 V arba 3 V).
Įkraunamą akumuliatorių galima įkrauti praleidžiant per jį elektros srovę atgal; tada jį vėl galima naudoti mažesniam arba didesniam elektros kiekiui gaminti. Šias įkraunamas baterijas 1859 m. išrado prancūzų mokslininkas Gaston Planté — jis sukūrė pirmąją praktišką švino rūgštinę bateriją. Vėliau atsirado daug kitų įkraunamų tipų, kurių savybės gerėjo: NiCd (nikelio–kadmio), NiMH (nikelio–metalo hidrido), Li-ion (ličio jonų) ir LiPo (ličio polimerų) akumuliatoriai, kuriuos šiandien plačiai naudoja elektronikoje ir transporto priemonėse.
Kaip veikia akumuliatoriai
Akumuliatorius susideda iš dviejų elektrodo medžiagų (anodo ir katodo) ir elektrolyto, kuris leidžia jonams judėti tarp jų. Kai grandinė uždaroma, vyksta oksidacijos ir redukcijos reakcijos: vienas elektrodas atiduoda elektronus (oksidacija), kitas priima (redukcija). Elektronų srautas per išorinę grandinę — tai elektros srovė. Įkrovimo metu šis procesas vyksta priešinga kryptimi (esant tam tikroms baterijų cheminėms savybėms), atstatant pradinę cheminę būseną.
Dažniausi akumuliatorių tipai ir jų savybės
- Neįkraunami (pirminiai) elementai: cinko–anglies (pigus, maža talpa), alkaliniai (dideli šiuolaikiniai vienkartiniai elementai), ličio vienkartiniai (ilgai laiko laikantis, didelė energijos tankis).
- Įkraunami (antriniai) akumuliatoriai: švino rūgštiniai (automobilio akumuliatoriai — didelė srovė paleidimui), NiCd (atsparūs temperatūros pokyčiams, bet turi nuodingą kadmį), NiMH (geresnė talpa nei NiCd, mažesnis atminties efektas), ličio jonų ir ličio polimero (aukštas energijos tankis, mažesnis svoris, šiandien populiariausi telefonuose, nešiojamuose kompiuteriuose, elektros automobiliuose).
Pagrindiniai techniniai parametrai
- Talpa: matuojama ampervalandomis (Ah) arba miliampervalandomis (mAh) — rodo, kiek srovės baterija gali tiekti tam tikrą laiką.
- Nominali įtampa: priklauso nuo chemijos (pvz., 1,5 V alkaliniams, ~2 V švino rūgštiniams, 3,6–3,7 V ličio jonams).
- Energijos tankis: kiek energijos galima sutalpinti į vienetą masės arba tūrio — svarbu nešiojamiems įrenginiams ir transportui.
- Ciklo trukmė ir ilgaamžiškumas: kiek kartų akumuliatorius gali būti įkraunamas ir iškraunamas prieš prarandant reikšmingą talpą.
- Savisiurbis: energijos praradimo greitis stovint — įvairūs tipai turi skirtingą savaiminio išsikrovimo lygį.
Saugumas, priežiūra ir perdirbimas
Saugumas: kai kurios baterijų chemijos (pvz., ličio jonai) gali būti užsidegančios ar sprogti esant pažeidimams, netinkamam krovimui arba perkaitus. Neapdorotos arba pažeistos baterijos neturėtų būti trumpai sujungtos arba ardytos. Visada naudokite tinkamą įkroviklį, skirtą konkrečiam akumuliatoriui.
Priežiūra: švino rūgštinius akumuliatorius reikėtų tikrinti skysčio lygius (kai kuriems tipams) ir apsaugoti nuo gilios iškrovos; ličio akumuliatoriams svarbu vengti per didelio įkrovimo ir per didelės iškrovos bei ekstremalių temperatūrų.
Perdirbimas ir aplinkosauga: daugeliu atvejų baterijos turi būti perduodamos specialioms atliekų surinkimo vietoms arba perdirbimo centrams, nes jose gali būti švino, kadmio, nikelio ar kitų pavojingų medžiagų. Teisingas šių atliekų tvarkymas sumažina taršą ir leidžia atgauti vertingus metalus.
Istorija trumpai
Pirmasis elektros šaltinis buvo Voltos elemtentas (Voltaic pile), sukurtas Alessandro Volta XIX a. pradžioje — tai buvo vienas pirmųjų cheminės energijos keitiklių. Vėliau, 1859 m., prancūzų inžinierius Gaston Planté išrado pirmąją praktišką daugkartinę švino rūgštinę bateriją. Per XX a. vystėsi naujos chemijos: Waldemar Jungner 1899 m. sukūrė NiCd elementą, vėliau atsirado NiMH, o XX a. pabaigoje ir XX a. pabaigoje — ličio pagrindu veikiantys akumuliatoriai, kurie tapo pagrindiniu energijos šaltiniu daugelyje nešiojamų ir stacionarių sistemų.
Panaudojimas
Akumuliatoriai naudojami labai plačiai: mažiems vartotojiškiems prietaisams (nuotolinio valdymo pultai, žaislai), elektronikai (telefonai, nešiojami kompiuteriai), transportui (automobilių starteriai, hibridiniai ir elektriniai automobiliai), stacionariems energijos kaupikliams (atsarginėms ir saulės energijos sistemoms) bei specialiai įrangai, pavyzdžiui, povandeniniams laivams, kur reikalinga didelė energijos talpa ir patikimumas.
Renkantis bateriją, verta įvertinti jos chemiją, talpą, nominalią įtampą, saugumo reikalavimus ir galimybes perdirbti — tai padės pasirinkti tinkamiausią sprendimą tiek kasdieniams prietaisams, tiek pramoniniams ar transporto poreikiams.