Cheminė reakcija vyksta tada, kai viena ar daugiau cheminių medžiagų virsta viena ar daugiau kitų cheminių medžiagų. Pavyzdžiai:
- geležis ir deguonis jungiasi į rūdis.
- actas ir geriamoji soda susijungia į natrio acetatą, anglies dioksidą ir vandenį.
- degantys arba sprogstantys daiktai.
- daugybė reakcijų, vykstančių gyvų organizmų viduje.
- elektrocheminės reakcijos iškraunant arba įkraunant akumuliatorius.
Vienos reakcijos yra greitos, kitos - lėtos. Kai kurios vyksta skirtingu greičiu, priklausomai nuo temperatūros ar kitų dalykų. Pavyzdžiui, šalta mediena nereaguoja su oru, tačiau, jei ją pakankamai įkaitinsime, ji pradės degti. Kai kurių reakcijų metu išsiskiria energija. Tai egzoterminės reakcijos. Kitų reakcijų metu energija yra gaunama. Tai endoterminėsreakcijos.
Branduolinės reakcijos nėra cheminės reakcijos. Cheminėse reakcijose dalyvauja tik atomų elektronai; branduolinėse reakcijose dalyvauja atomo branduolio protonai ir neutronai.
Ką reiškia cheminė reakcija iš esmės?
Cheminėje reakcijoje pradinės medžiagos (reaktantai) perima elektronus, sudaro arba laužo cheminius ryšius ir taip susidaro naujos medžiagos (produktai). Reakcijos metu galioja atomų ir masės išsaugojimo dėsnis: atomų skaičius prieš ir po reakcijos nesikeičia, todėl chemines reakcijas žymime subalansuotomis cheminėmis lygtimis.
Pavyzdžiai lygtimis:
- Acto ir geriamųjų sodų reakcija: CH3COOH + NaHCO3 → CH3COONa + CO2 ↑ + H2O
- Geležies rūdijimas (supaprastinta): 4 Fe + 3 O2 → 2 Fe2O3
Cheminės reakcijos pagrindiniai požymiai
- Ryšių peržaidimas: susidaro nauji cheminiai ryšiai ir yra suardomi seni.
- Energijos pokyčiai: išsiskyrimas (egzoterminės) arba absorbcija (endoterminės), dažnai matomi kaip temperatūros pokytis, šviesa ar garsas.
- Spalvos, kvapo ar dujų išsiskyrimas: kartais pasikeičia reagentų spalva arba susidaro naujas kvapas; pavyzdžiui, CO2 burbuliukai acto ir sodos mišinyje.
- Nuosėdos susidarymas: kai produktas yra netirpūs junginiai (precipitacija).
Cheminių reakcijų tipai (trumpai)
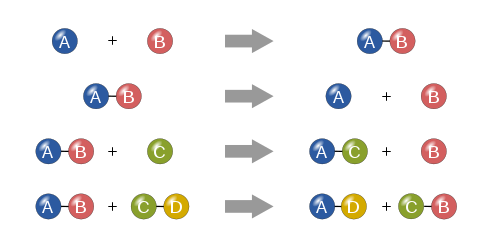
- Sintezė (kombinacija): du arba daugiau reagentų susijungia į vieną produktą (A + B → AB).
- Skaidymas (dekompozicija): vienas junginys skyla į paprastesnes dalis (AB → A + B).
- Vienvietis pakeitimas (metatezė): vienas atomų ar jonų pakeičia kitą (A + BC → AC + B).
- Dviejų vietų pakeitimas (dviguba metatezė): jonai keičiasi vietomis (AB + CD → AD + CB), dažnai matoma druskų tirpimo ir nuosėdų formavimo procesuose.
- Degimas (kombustija): reakcijos su deguonimi, dažnai greitos ir egzoterminės; pavyzdys — organinių medžiagų degimas.
- Redoks reakcijos: vyksta elektronų pernaša (oksidacija ir redukcija).
- Acidų ir bazių reakcijos: protonų pernaša, neutralizacija (H+ + OH− → H2O).
- Polimerizacija: mažos molekulės susijungia į dideles polimerines grandines.
Veiksniai, lemiantys reakcijos greitį
- Temperatūra: didesnė temperatūra paprastai didina dalelių kinetinę energiją ir reakcijų greitį.
- Koncentracija: didesnė reagento koncentracija didina susidūrimų tikimybę.
- Paviršiaus plotas: kietų dalelių smulkinimas (didesnis plotas) pagreitina reakcijas su tirpikliu ar oru.
- Slėgis: svarbu dujų reakcijoms — didesnis slėgis gali padidinti reakcijų greitį.
- Katalizatoriai: medžiagos, kurios mažina aktyvacinę energiją ir pagreitina reakciją, bet nešvaisto paties katalizatoriaus.
- Šviesa: fotocheminės reakcijos vyksta apšvietus (pvz., fotosintezė, fotochemija).
Reversiškumas ir cheminė pusiausvyra
Daugelis reakcijų yra grįžtamos — produktai gali reaguoti atgal į reagentus. Kai į priekį ir atgal vykstančių procesų greičiai susilygina, susidaro dinaminė cheminė pusiausvyra. Pusiausvyros padėtį nulemia koncentracijos, temperatūros ir slėgio pokyčiai (Le Châtelier principas).
Cheminės ir fizinės reakcijos skirtumai
Cheminė reakcija reiškia medžiagų cheminį perskirstymą ir naujų medžiagų susidarymą. Fiziniai pokyčiai (pvz., lydymas, garavimas) nekeičia medžiagų cheminės sudėties — tik būseną ar formą.
Praktinė reikšmė ir sauga
Cheminės reakcijos yra kasdienio gyvenimo dalis: gaminame maistą, kuras, medikamentus, sintetinius polimerus, valiklius, ir kt. Daugelis pramoninių procesų priklauso nuo efektyvių ir saugių cheminių reakcijų. Tačiau kai kurios reakcijos gali būti pavojingos (sprogimai, toksiški dujų išsiskyrimai, stiprus šilumos išsiskyrimas), todėl svarbu laikytis saugos priemonių: naudoti tinkamą apsaugos įrangą, vėdinimą ir saugias darbo procedūras.
Pastaba apie branduolines reakcijas
Kaip nurodyta aukščiau, branduolinės reakcijos nėra cheminės reakcijos — jose keičiasi atomo branduolio sudėtis (protonai, neutronai), o cheminėse reakcijose pokyčiai vyksta elektronų lygmenyje (elektronai).
Jeigu norite, galiu pateikti iliustracijas ar paprastus uždavinius apie reakcijų balansavimą, katalizatorių veikimą ar paaiškinti konkrečių pavyzdžių mechanizmus detaliau.