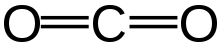Anglies dioksidas (CO2) yra cheminis junginys. Kambario temperatūroje jis yra dujos. Jį sudaro vienas anglies ir du deguonies atomai. Žmonės ir gyvūnai iškvėpdami išskiria anglies dioksidą. Be to, kiekvieną kartą, kai deginamas koks nors organinis daiktas (arba kuriama ugnis), išsiskiria anglies dioksidas. Augalai anglies dioksidą naudoja maistui gaminti. Šis procesas vadinamas fotosinteze. Anglies dioksido savybes ištyrė škotų mokslininkas Džozefas Blekas (Joseph Black) XVIII a. viduryje.
Anglies dioksidas yra šiltnamio efektą sukeliančios dujos ir prisideda prie to, kad atmosfera sulaiko šilumos energiją. Šiltnamio efektą sukeliančios dujos keičia mūsų planetos — Žemės — klimatą ir orus. Šis procesas vadinamas klimato kaita ir yra viena iš pagrindinių visuotinio atšilimo — Žemės paviršiaus temperatūros kilimo — priežasčių.
Fizinės ir cheminės savybės
Anglies dioksidas yra bespalvės, bekvapės dujos. Jų molinė masė (44 g/mol) yra didesnė už oro (~29 g/mol), todėl CO2 yra maždaug 1,5 karto sunkesnis už orą ir linkęs kauptis žemose vietose. Esant žemai temperatūrai ir aukštam slėgiui, CO2 gali susikondensuoti arba sublimuoti į kietą formą („sausesnis ledas“) — jis sublimuojasi ties −78,5 °C. Vandenyje ištirpęs anglies dioksidas dalinai virsta anglies rūgštimi (H2CO3), todėl tirpalas tampa rūgštesnis.
Šaltiniai ir ciklas
Natūralūs CO2 šaltiniai: vulkanai, dirvožemio kvėpavimas, skaidymosi procesai, vandenynai, kuriuose išsiskiria anglies dioksidas dalinai dėl biologinių ir cheminių procesų. Žmonių veikla (antropogeniniai šaltiniai) — žymiai padidinusi atmosferinę CO2 koncentraciją — apima:
- fossilinių kuro (anglies, naftos, dujų) deginimą;
- pramoninius procesus, ypač cemento gamybą (kalcinacija išlaisvina CO2 iš kalkakmenio);
- miškų kirtimą ir žemės paskirties pakeitimus, kurie mažina augalų gebėjimą įsisavinti CO2.
Anglies dioksidas dalyvauja anglies cikle: fotosintezės metu augalai sugeria CO2, o kvėpavimas, skaidymasis ir deginimas grąžina jį į atmosferą. Dalis antropogeninio CO2 absorbuojama vandenynų ir biomase; dalis lieka atmosferoje dešimtmečius ar šimtmečius.
Poveikis klimatui ir aplinkai
CO2 stiprina natūralų šiltnamio efektą — absorbuodamas infraraudonąją spinduliuotę, jis mažina išsiskiriamos šilumos kiekį į kosmosą. Dėl to atmosfera ir Žemės paviršius šyla. Nuo industrializacijos pradžios atmosferos CO2 koncentracija išaugo nuo apie 280 ppm iki maždaug 420 ppm (pastaraisiais dešimtmečiais), o tai smarkiai prisideda prie klimato kaitos.
CO2 emisijos sukelia keletą tarpusavyje susijusių pasekmių:
- temperatūros kilimas ir ekstremalesni orų reiškiniai (karščio bangos, liūtys, audros);
- jūros lygio kilimas dėl ledynų tirpimo ir terminio vandens plėtimosi;
- ekosistemų ir žemės ūkio pokyčiai, augalų fenologijos (žydėjimo, derliaus laikai) pasikeitimai;
- vandenynų rūgštėjimas: tirpdantis CO2 mažina jūrų vandens pH, o tai kenkia koralams, moliuskams ir kitoms organizmų, kuriems reikalingos kalkinės struktūros.
Sveikata ir sauga
Atmosferoje esančio CO2 koncentracijos įprastomis sąlygomis (~400 ppm) nereikia bijoti — kitu atveju jis yra natūrali gyvenimo dalis. Tačiau didesnės koncentracijos uždaroje patalpoje (pvz., virš ~1 000 ppm) rodo prastą vėdinimą ir gali sukelti galvos skausmą, nuovargį ir sumažėjusį produktyvumą. labai aukštos koncentracijos (dešimtys tūkstančių ppm) gali būti pavojingos ar mirtinos, nes CO2 gali išstumti deguonį.
Ką galime daryti (mažinimo priemonės)
Siekiant sumažinti atmosferos CO2 koncentraciją ir sulėtinti klimato kaitą, taikomos kelios strategijos:
- energijos gamybos pereiga prie atsinaujinančių išteklių (saulės, vėjo, hidro);
- energetinis efektyvumas ir vartojimo mažinimas;
- miškų atkūrimas ir apsauga, dirvožemio anglies kaupimo skatinimas;
- technologijos šiltnamio dujų mažinimui: anglies surinkimas ir saugojimas (CCS), anglies fiksavimas dirvožemyje ir kt.;
- pramoninių procesų keitimas ir emisijų reguliavimas.
Santrauka
Anglies dioksidas (CO2) yra natūrali ir būtina biosferos dalis: jis dalyvauja fotosintezėje ir anglies cikle. Tačiau didėjanti antropogeninė CO2 emisija stiprina šiltnamio efektą, keičia klimatą, skatina ekstremalesnius orus ir sukelia vandenynų rūgštėjimą. Sumažinti emisijas ir skatinti anglies kaupimą aplinkoje — vienas pagrindinių žmogiškosios veiklos iššūkių siekiant stabilizuoti klimatą ir apsaugoti ekosistemas.