Organinėje chemijoje eliminacijos reakcija yra procesas, kai iš didesnės molekulės pašalinami vienas ar keli atomai arba atomų grupės. Dažnai tokių reakcijų rezultatas – susidariusi dviguba arba triguba jungtis, t. y. teks rasti naują neįsitvirtinusių jungčių sistemą molekulėje.
Mechanizmo pagrindai: E1 ir E2
Yra du pagrindiniai eliminacijos mechanizmai, dažnai žymimi E1 ir E2.
E1 mechanizmas vyksta dviem etapais. Pirmiausia išeina gera paliekamoji grupė ir susidaro tarpinis karbokationas; vėliau bazė arba kita bazinė medžiaga atima vandenilio joną iš gretimo anglies atomo, susidarant dvigubai jungčiai. E1 reakcijos dažnai lėtesnės, jų greitis priklauso tik nuo substrato koncentracijos (atitinka pirmo laipsnio kinetiką) ir yra palankios, kai karbokationas yra stabilus (pvz., terciniai angliavandeniliai).
E2 mechanizmas yra vieno žingsnio procesas: stipri bazė vienu metu atima protoną, kai paliekamoji grupė išeina, todėl susidaro dviguba jungtis be tarpinio karbokationo. E2 reakcijos greitis priklauso nuo substrato ir bazės koncentracijų (antras laipsnis), paprastai vyrauja esant stiprioms bazėms ir esant tinkamai geometrijai tarp atimamo vandenilio ir išeinančios grupės (antiperiplanarinė sandara).
Praktiniai pavyzdžiai
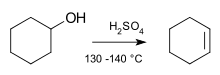
Dažnas eliminacijos atvejis yra dehidracija, kai iš alkoholiais pašalinama vandens molekulė, pavyzdžiui, rūgštiniame bei šildomame terpėje – taip gaunamos alkenai. Kitas dažnas pavyzdys – dehidrohalogenacija, kai iš alkilhalogenidų išeina halogenas ir vyksta dvigubos jungties formavimas.
Faktoriai, lemiantys mechanizmą
- Substrato struktūra: terciariniai centrai palankesni E1 (karbokationo stabilumas), primariniai dažniau E2 (E1 karbokationui nestabilus).
- Paliekamoji grupė: gera paliekamoji grupė (pvz., halogenidai) palengvina tiek E1, tiek E2; blogos (pvz., −OH be aktyvacijos) gali reikalauti kitų mechanizmų (E1cB arba rūgštinės aktyvacijos).
- Bazės stiprumas: stiprios bazės skatina E2; silpnos bazės ir polinė protinė terpė gali skatinti E1.
- Terpė: polinės protinės medžiagos stabilizuoja karbokationus → E1 palankesnė.
- Temperatūra: aukštesnė temperatūra dažnai skatina eliminaciją prieš substituciją.
Regio- ir stereocheminiai aspektai
- Regioselekyvumas: daugeliu atvejų eliminacijoje susidaro termodinamiškai stabilesnis, labiau alkilintas alkenas (Zaitsevo taisyklė). Tačiau didelės, steriškai užimtos bazės gali duoti Hofmano produktą (mažiau alkilintą alkeną).
- Stereocheminė kontrolė: E2 yra stereospecifinė reakcija – vandenilis, kurį atima bazė, ir išeinanti grupė turi būti antiperiplaniniai (ypač akivaizdu ciklinėse struktūrose, pvz., cikloheksane reikia, kad išeinanti grupė būtų ašinė). E1 mechanizme dėl tarpinio karbokationo galima gaudyti racemizaciją ir produktų mišinį.
- Permainos (rearrangements): E1 gali lydėti karbokationo perėjimai (hidridų ar alkilų perėjimai), kurie keičia galutinio alkeno poziciją; E2 tokių perėjimų neturi.
Konkuruojančios reakcijos ir alternatyvos
- Substitucija (SN1/SN2): esant tam tikroms sąlygoms (silpna bazė, geras nukleofilas), eliminacija gali konkuruoti su substitucija. Pvz., terpėje ir su silpna baze gali vykti SN1 kartu su E1; su stipria nukleofile/baze ir primariniu substratu dažna SN2 arba E2 (esant stipriai bazei – E2).
- E1cB mechanizmas: kai paliekamoji grupė yra bloga (pvz., −OH be aktyvacijos) arba kai susidaro stabilus karbanionas (pvz., konjugacija su elektroną atitraukiančia grupe), eliminacija gali vykti per anioninį tarpinį produktą: pirmiausia bazė atima protoną, susidaro karbanionas, o vėliau išeina paliekamoji grupė.
Praktiniai patarimai laboratorijoje
- Jei norima skatinti eliminaciją vietoje substitucijos, naudokite stipresnes bazes, aukštesnę temperatūrą ir polarų aprotinį arba protinį terpę, priklausomai nuo pageidaujamo mechanizmo.
- Sekite stereochemines reikalavimus (ypač cikliniuose junginiuose) – E2 reikalauja tinkamos konformacijos (antiperiplanarinės).
- Jei substratas gali sudaryti stabilų karbokationą ir pastebite produktų perėjimus, galimai veikia E1 su permainomis.
Santrauka: eliminacijos reakcijos (E1 ir E2) yra svarbi organinės sintezės dalis, leidžianti išvesti alkenus ir alkinus. Renkantis sąlygas būtina įvertinti substrato tipą, bazės stiprumą, paliekamosios grupės kokybę, terpę ir temperatūrą, nes nuo to priklausys, ar vyks E1, E2, E1cB ar konkuruojanti substitucija.