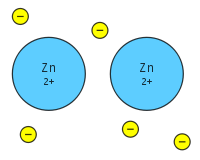
Metalinė jungtis – tai ryšio tarp atskirų metalo atomų forma, kai daugelio atsiskyrusių elektronų dalijimasis tarp daugelio teigiamų jonų, sukuria delokalizuotą elektronų „jūrą“, kuris veiksmingai „klijuoja“ teigiamus jonų režius kartu. Skirtingai nei kovalentinis ar joninis ryšys, metalinėje jungtyje valentiniai elektronai nėra susieti su konkrečiais atomais, o gali laisvai judėti per visą kristalinę gardelę. Dėl to daugelis metalų pasižymi specifinėmis fizinėmis ir cheminėmis savybėmis.
Veikimo principas
Metalinės jungties pagrindas – delokalizuotų elektronų koncentracija ir jų trauka teigiamai įkrautoms metalų atomų joninėms dalims. Metalų atomų išoriniai energijos lygmenys (atominės orbitalės) persidengia, todėl elektronai nėra lokalizuoti. Šis persidengimas leidžia elektronams formuoti bendrą elektronų debesį arba „jūrą“, kuri supa teigiamus jonus. Tokia sistema suteikia stabilumą visai kristalinei struktūrai ir paaiškina metalo atsparumą deformacijai bei jo cheminį elgesį.
Metalinės jungties stiprumas priklauso nuo keleto veiksnių:
- valentinių elektronų skaičiaus (daugelis laisvų elektronų – stipresnis tarpusavio ryšys),
- atomų spindulio ir jų tarpusavio atstumo kristalinėje gardelėje,
- elektronų delokalizacijos lygio – stipresnis persidengimas didina jungties stiprumą,
- elektronų ir branduolių traukos jėgos dydžio (susijusios su metalų jonizacijos energija).
Metalinės jungties pasekmės – pagrindinės savybės
Metalinės jungtys lemia daug specifinių metalo savybių:
- Elektrinis laidumas: laisvi delokalizuoti elektronai sudaro tinkamą terpę, per kurią lengvai praeina elektros srovė. Dėl to metalai yra geri laidininkai.
- Šilumos laidumas: elektros laidumo mechanizmas taip pat palengvina šilumos perdavimą – laisvi elektronai greitai perneša kinetinę energiją.
- Blizgesys: metalo elektronai sugeria ir greitai reemitina šviesą, dėl to metalai yra blizgūs.
- Plastiškumas ir tašumas: sluoksniai metalo atomų gali slysti vienas kito atžvilgiu, nes elektronų „jūra“ palaiko ryšį net ir keičiantis atstumams. Dėl to metalai dažnai būna plastiški (galima juos kaldinti, stumdyti) ir tuo pačiu metu tam tikru mastu tašūs.
- Aukštos lydymosi ir virimo temperatūros: stipri trauka tarp elektronų ir teigiamų jonų reiškia, kad reikalinga daug energijos, kad būtų nutraukta medžiagos tvarka ir pereita į skystą ar garinį būvį.
- Mikrostruktūrinės savybės: metalų stiprumas, kietumas ir atsparumas smūgiams priklauso nuo kristalinės gardelės tipo, dislokacijų buvimo ir kitų defektų, taip pat nuo elektronų koncentracijos.
Modeliai ir paaiškinimai
Metalinio ryšio elgesį galima aprašyti keliais modeliais:
- Elektronų jūros modelis: supaprastintas modelis, kuriame valentinių elektronų skaičius traktuojamas kaip laisvųjų elektronų dujos, o teigiami jonai – fiksuoti fonas.
- Bandų teorija: kvantinė kietųjų medžiagų teorija, paaiškinanti laidumą ir puslaidininkiškumą kaip elektrono energetinių lygmenų susidarymą didelėse sistemose; metaluose valentinės ir laidumo juostos persidengia arba laidumo juosta yra užpildyta tik iš dalies, todėl egzistuoja laisvi elektronai.
- Drudės modelis: klasikinis požiūris į elektronų judėjimą ir laidumą, naudingas aptariant atsparumą ir temperatūros priklausomybę.
Išimtys ir ypatumai
Ne visi metalai elgiasi vienodai. Pavyzdžiui, pereinamieji metalai turi dalinius d-orbitalių indėlius, kas gali stiprinti arba komplikuoti metalinį ryšį ir lemti didesnį kietumą bei aukštesnes lydimosi temperatūras. Taip pat yra medžiagų, kurios nėra metalai tradicine prasme, bet praleidžia elektrą – pavyzdžiui, grafitas, nes, panašiai kaip metalai, turi dalokalizuotus elektronus. Joniniai junginiai gali būti laidūs tik tada, kai ištirpę arba išlydyti (laisvi jonai gali judėti).
Kai kurie junginiai ar jonų poros gali formuoti kitas jungčių rūšis; pavyzdžiui, ne visi metalų tarpusavio sąveikos tipai būna grynai metaliniai. Pavyzdžiui, gyvsidabrio jonai (Hg2+
2)) gali sudaryti kovalentines metalo–metalo jungtis tam tikrose sąlygose.
Metalinės jungties reikšmė pramonėje ir technologijose
Metalinė jungtis ir su ja susijusios savybės yra lemiamos medžiagų parinkimo inžinerijoje: laidumas – elektros ir elektronikos komponentams, šilumos laidumas – šiluminių keitiklių ir šiluminės valdymo sistemoms, plastiškumas – apdirbimui (kalimas, štampavimas, stūmimas). Keistas metalų cheminis elgesys ir galimybė formuoti lydinius suteikia plačias galimybes medžiagų savybių optimizavimui.
Lydiniai
Lydinys yra metalų tirpalas arba šeima mišinių, kuriuose keli metalai (kartais su nemetalais) sumaišyti atominiu lygiu. Lydiniai dažnai turi geresnes mechanines savybes, didesnį atsparumą korozijai arba žemesnę lydymosi temperatūrą nei gryni metalai. Dauguma lydinių yra blizgūs kaip ir gryni metalai, tačiau jų mechaninės savybės gali smarkiai skirtis priklausomai nuo sudėties ir mikrostruktūros.
Santrauka
Metalinė jungtis – tai delokalizuotų elektronų ir teigiamų metalinių jonų traukos reiškinys, kuris paaiškina daugelį metalo fizinių savybių: elektrinį ir šiluminį laidumą, blizgesį, plastiškumą, aukštas lydymosi temperatūras ir kt. Skirtingų metalų charakteristikos priklauso nuo elektronų skaičiaus, orbitalių persidengimo ir kristalinės struktūros, o lydiniai leidžia šias savybes pritaikyti konkretiems technologiniams poreikiams.