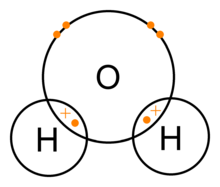
Kovalentiniai ryšiai – tai cheminiai ryšiai, kurie susidaro tarp dviejų nemetalo atomų, kai atomai dalijasi valentiniais elektronais. Pavyzdys – vanduo, kuriame vandenilis (H) ir deguonis (O) susijungia į (H2O). Daugeliui elementų „pilnas“ išorinis elektronų sluoksnis reiškia aštuonis elektronus (tai vadinama oktetine taisykle), o vandeniliui ar heliui užtenka dviejų. Valentiniai elektronai – tai elektronai, esančius atomo išoriniame sluoksnyje ir dalyvaujantys ryšiuose. Elektronų apvalkalų išsidėstymą lemia kvantinė mechanika, todėl skirtingi elementai linkę formuoti skirtingus ryšių tipus.
Kaip susidaro kovalentinis ryšys
Atomo elektronų skaičių lemia protonų skaičius branduolyje. Elektronai skrieja aplink branduolį apibrėžtomis kvantinėmis orbitalėmis; pirmajame sluoksnyje telpa iki dviejų elektronų, tolimesniuose – dažniausiai iki aštuonių (pagal oktetą). Kovalentinis ryšys susidaro tuomet, kai du atomai dalijasi vienu arba daugiau elektronų porų, kad kiekvienam atomui suteikti arčiau pilną išorinį sluoksnį.
Fizikinis paaiškinimas gali būti trumpai pateiktas taip: kai laisvai laikomas elektronas iš vieno atomo „pereina“ į bendrą orbitalę, susietą su abiejų atomų branduoliais, bendras sistemos energijos lygis sumažėja. Energija, sumažėjusi formuojant ryšį, gali išsiskirti įvairiomis formomis (pvz., šiluma arba elektromagnetiniu spinduliavimu). Elektronų bendrinimas sukuria sąlyginius dalinius įkrovimus (δ+ ir δ–), o atomus sulaiko elektromagnetinė trauka – taip ir susidaro stabilus kovalentinis ryšys. Ryšį nutraukti reikia tiek energijos, kiek jos išsiskyrė jį sudarant (tai vadinama ryšio lūžio energija).
Ryšių tipai ir jų savybės
- Viengubas, dvigubas ir trigubas ryšiai: viengubas – viena elektronų pora (pvz., H–H), dvigubas – dvi poros (pvz., O=O), trigubas – trys poros (pvz., N≡N). Kuo didesnė ryšio eilė, tuo trumpesnis ir stipresnis ryšys.
- Ne polinis (nesimetrinis) ir polinis ryšys: jei atomai yra to paties ar labai panašaus elektronegatyvumo, elektronai dalijami simetriškai – gaunamas nepolinis kovalentinis ryšys (pvz., H2, Cl2). Jei elektronegatyvumas skiriasi, elektronų debesys juda arčiau labiau elektronegatyvaus atomo ir susidaro polinis kovalentinis ryšys (pvz., H–O vandenyje). Poliniame ryšyje vienas atomas įgauna dalinį neigiamą krūvį (δ–), kitas – dalinį teigiamą (δ+).
- Koordinacinis (doinės) kovalentinis ryšys: kai abu bendros elektronų poros elektronai suteikiami vieno atomo (pvz., NH4+ susidarymas arba kompleksai su pereinamaisiais metalais).
- Tinklinis (tinklinis kovalentinis) ryšys: kai atomas jungiasi daugeliu kovalentinių ryšių į didelį tinklą – pvz., deimantas (grynas anglies tinklas) ar silicio dioksidas (SiO2). Tokie junginiai būna labai kieti ir turi aukštą lūžio energiją.
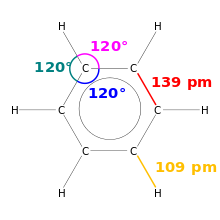
- Rezonavimas: kai elektronai gali būti perkelti tarp kelių orientalinių struktūrų (pvz., benzene), faktinis elektronų pasiskirstymas yra vidutinė būsenų kombinacija, o tai stabilizuoja molekulę.
Pavyzdžiai
- H2 – paprastas nepolinis viengubas ryšys tarp dviejų vandenilio atomų.
- O2 – turi dvigubą ryšį; dalyvauja ne tik σ, bet ir π orbitalės.
- N2 – trigubas ryšys, labai stiprus ir trumpas, todėl N≡N molekulinė azoto jungtis yra stabiliausia.
- Vanduo, kur deguonis yra žymiai elektronegatyvesnis už vandenilį (H), todėl deguonis įgauna dalinį neigiamą krūvį (δ–), o vandeniliai – dalinį teigiamą (δ+). Dėl to H2O molekulė yra polinė, o tai lemia daug vandens savybių (pvz., didelę lydymosi/virimo temperatūrą, tirpumą poliniuose tirpikliuose).
- CH4 – anglies ir vandenilio ryšiai yra gana nepoliniai dėl mažo elektronegatyvumo skirtumo, todėl CH4 yra apvalios simetrijos ir nepolinė molekulė.
- CO – turi stiprų polinį trigubą ryšį su didele cheminės kompleksų aktyvumo reikšme (vartojama koordinaciniuose kompleksuose).
- Tinklinės struktūros: deimantas (grynas anglies tinklas) ir kvarcas (SiO2) – pavyzdžiai, kur kovalentiniai ryšiai sudaro didelį 3D tinklą.
Kovalentinio ir ioninio ryšio skirtumai
Trumpai: kovalentinis ryšys – elektronų dalijimasis; ioninis ryšys – elektronų perdavimas ir jėgos tarp priešingų jonų. Ryšio pobūdis dažnai priklauso nuo elektronegatyvumo skirtumo: mažas skirtumas → kovalentinis; didelis skirtumas → ioninis. Tarpiniai atvejai duoda polinius kovalentinius junginius.
Praktinė reikšmė
Kovalentiniai ryšiai yra pagrindas organinei chemijai, biologinėms molekulėms (baltymai, DNR, angliavandeniliai), medžiagų inžinerijai (puslaidininkiai, polimerai ir kt.) bei kasdieniam cheminiam poveikiui. Supratimas apie ryšio tipą ir jo stiprumą padeda prognozuoti junginio savybes – formą, reaktoriškumą, tirpumą ir termodinamines charakteristikas.