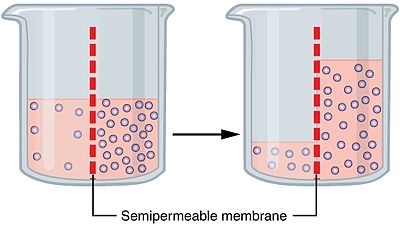
Osmozė – tai vandens judėjimas per pusiau pralaidžią membraną iš regiono, kuriame tirpalo (tirpiklio) koncentracija yra didesnė vandens (t. y. mažesnė tirpalo koncentracija), į regioną, kuriame tirpalo koncentracija yra didesnė, siekiant sumažinti koncentracijos skirtumą. Kitaip sakant, vanduo juda iš zonos su mažesne ištirpusių dalelių koncentracija į zoną su didesne ištirpusių dalelių koncentracija. Osmozė yra pasyvioji pernaša – jai nereikalinga tiesioginė energija (ATP), nors ją nulemia priešingų jėgų pusiausvyra, kaip hidrostatinis slėgis ir aktyvus jonų pernašos poveikis. Osmotinį slėgį sukelia skirtinga tirpiųjų medžiagų koncentracija abiejose membranos pusėse.
Mechanizmas ir paaiškinimas
Per pusiau pralaidžią membraną praeina daugiausia mažesni tirpiklio molekulių arba tirpiklis nepraleidžiamas visiškai, tačiau vandens molekulės gali praeiti. Vanduo juda kryptimi, kuri sumažina cheminių potencialų skirtumą. Praktiniu požiūriu tai reiškia, kad vanduo pereina iš mažesnės tirpiklio (didžiausio vandens) koncentracijos į didesnę tirpiklio (mažesnio vandens) koncentracijos pusę, kol susiformuoja pusiausvyra tarp osmosinio ir hidrostatinio slėgių.
Osmotinis slėgis ir termodinaminė formulė
Osmotinį slėgį galima kiekybiškai apibrėžti. Paprastame atvejyje jis aprašomas van ’t Hoff lygtimi: π = iCRT, kur
- π – osmotinis slėgis,
- i – dalelių disociacijos faktorius (Van ’t Hoff koeficientas),
- C – molinis tirpalo molarumas,
- R – universali dujų konstanta,
- T – absoliuti temperatūra (Kelvinais).
Tai užuominai, kad osmozė yra koligatyvinė savybė – priklauso ne nuo konkrečių tirptųjų medžiagų cheminių savybių, o nuo jų skaičiaus tirpale.
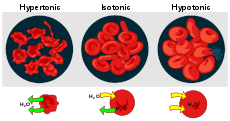
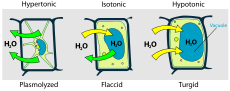
Terminoligija: izotoninis, hipotoniškas, hipertoninis
- Izotoninis tirpalas – turi tokią pačią tirpalų koncentraciją kaip ląstelės vidus; vandens srautas į abi puses yra subalansuotas.
- Hipotoninis tirpalas – išorinė terpė turi mažesnę tirpiklių koncentraciją nei ląstelė; vanduo juda į ląstelę → gali įvykti patinimas arba, gyvūninėms ląstelėms, hemolizė.
- Hipertoninis tirpalas – išorinė terpė turi didesnę tirpiklių koncentraciją; vanduo išeina iš ląstelės → ląstelė gali susitraukti (plazmolizė augaluose, krumpėjimas gyvūnų ląstelėse).
Poveikis ląstelėms
Osmozė yra lemiamas veiksnys ląstelių tūrio ir formos reguliavimui:
- Augalų ląstelėse turgorinis slėgis (vandens slėgis prieš ląstelės sienelę) palaiko augalo standumą ir yra svarbus augimo procesams. Per didelė ar per maža osmozinė būsena (pvz., ilga hipotoninė ar hipertoninė ekspozicija) sukelia plazmolizę arba praradimą turgoro.
- Gyvūnų ląstelėse, neturint kietos sienelės, stiprios osmosinės slėgio pokyčiai gali lemti ląstelės plyšimą arba susitraukimą (hemolizė arba krumpėjimas).
- Organizmuose egzistuoja osmoreguliaciniai mechanizmai (inkstai, specializuotos ląstelės, pumpuojančios jonus), kurie perkelia jonus aktyviai, keisdami osmosinį gradientą ir taip kontroliuodami vandens judėjimą.
Akvaporinai ir reguliacija
Akvaporinai – tai specialios baltymų kanalų formos, leidžiančios greitai ir selektyviai pratekėti vandeniui per membraną. Jie padidina membranos pralaidumą vandeniui ir jų ekspresija bei aktyvumas gali būti reguliuojamas pagal ląstelės poreikį (pvz., hormonų, kaip ADH inkstuose, poveikiu). Nors osmozė pati energijos nereikalauja, aktyvus jonų pernašos reguliavimas gali sukurti arba panaikinti osmosinius gradientus.
Biologinė ir praktinė reikšmė
- Osmozė yra fundamentali medžiagų ir vandens homeostazei, augalų fiziologijai, kraujo ir ląstelių tūrio reguliacijai.
- Medicinoje osmozė ir pusiau pralaidžios membranos principai taikomi hemofiltracijoje, dializėje ir vaistų formulavime (pvz., lašinio tirpalų izotoninės sudėties užtikrinimas).
- Pramonėje ir kasdienybėje osmozė yra naudojama atvirkštinės osmozės technologijose, skirtose vandens valymui ir jūros vandens gėlinimui, taip pat maisto pramonėje (koncentravimas, sūdymas) ir biologinių membranų tyrimuose.
Moksliniai ir eksperimentiniai aspektai
Laboratorijoje osmozę galima tirti stebint ląstelių elgseną skirtingose tirpalų koncentracijose, matuojant osmotinį slėgį osmomometru arba apskaičiuojant pagal van ’t Hoff lygtį idealizuotais atvejais. Realiuose tirpaluose reikia atsižvelgti į nestandartinį dissociacijos laipsnį, jonų sąveikas ir membranos pralaidumo skirtumus.
Apibendrinant, osmozė yra esminis fizikinis ir biologinis reiškinys, kurio supratimas leidžia paaiškinti ląstelių elgseną, organizmų homeostazę ir kurti technologijas, paremta pusiau pralaidžių membranų savybėmis.