Organinėje chemijoje adityvinė (adicioninė) reakcija – tai procesas, kai dvi molekulės susijungia į vieną, prijungiantis vienos molekulės atomus ar grupes prie kitos molekulės vietų, kurios turi dvigubą arba trigubą ryšį. Dažniausiai tai yra anglis–anglis dvigubi/trigubi ryšiai, bet adityvios reakcijos gali vykti ir prie anglis–deguonis, anglis–azotas ir kitų funkcinių grupių. Viena iš reaguojančių rūšių veikia kaip nukleofilas (perduoda elektronus), kita – kaip elektrofilas (priima elektronus).
Adityvinė reakcija yra priešinga eliminacijos reakcijai: eliminuojant išeina mažesnė molekulė arba grupė, adityvijoje prie nešvarumo (pvz., dvigubo ryšio) pridedama nauja fragmentų pora. Dažniausi praktiniai pavyzdžiai – vandens pridėjimas prie alkenų (hidratacija) arba nukleofilinės atakos prieš karbonilą (karbonilo nukleofilinė adicija).
Adityvinių reakcijų tipai ir mechanizmai
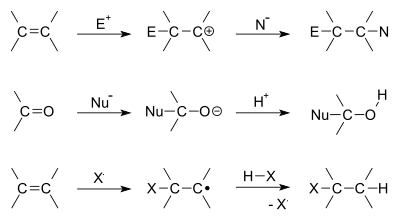
- Elektrofilinė adicija – dažna alkenų reakcija. Elektrofilas (pvz., H+, Br+) pirmiausia atakuoja dvigubą jungtį, susidaro tarpinis karbokationas arba bridžinis halonium jonas, o vėliau nukleofilas prijungiamas prie suformuotos centrinės rūšies. Pavyzdžiai: hidrohalogeninimas (HBr), halogeninimas (Br2), sūraus katalizė hidratacijai.
- Nukleofilinė adicija prie karbonilo – karbonilo anglis (elektrofilinė) gauna elektronus iš nukleofilo (pvz., R-MgBr, CN−, alkoholiai), susidaro alkoksido tarpinė rūšis, kuri vėliau protonuojama. Tai pagrindas Grignardo reakcijoms, ciano hidratacijai, hemiacetalų ir acetalių susidarymui.
- Radikalinė adicija – įvyksta per laisvųjų radikalų grandinę; svarbu polimerizacijose ir kai kurie hidrohalogeninimo atvejai (pvz., HBr prie alkenų esant peroksidams – anti‑Markovnikov produkcija).
- Periacinės ir pericyklinės adicijos – tai concerted (vienu etapu) procesai, pvz., Diels–Alder reakcija (dienas + dienofilas) su stereospesifiniu rezultatu.
- 1,2- ir 1,4-adicija (konjuguotų sistemų atvejai) – konjuguoti enonai gali patirti tiesioginę (1,2) arba atitrūkusią (1,4, Michael adicija) adiciją, priklausomai nuo sąlygų ir reaktantų charakterio.
Regiochemija ir stereochemija
Markovnikovo taisyklė nurodo, kad elektrofilas (pvz., H+) paprastai prijungiamas prie anglies, turinčios daugiau vandenilių, o nukleofilas – prie labiau alkilizuotos anglies, kad susidarytų stabilesnis karbokationas. Yra išimčių: anti‑Markovnikov addicijos pasiekiamos per radikalų mechanizmus arba naudojant hidroboraciją (vėliau oksidaciją).
Stereocheminė kryptis: adicijos gali būti syn (abu fragmentai prisijungia iš tos pačios plokštumos šono, pvz., katalitinė hidrogenacija) arba anti (priešinėse plokštumose, pvz., halogeninimas per bridžinį halonium joną). Kai mechanizmas vyksta per bridžinį tarpinių jonų, paprastai gaunama anti‑adicija; kai per metalinį katalizatorių arba concerted mechanizmą – sintezė gali duoti syn‑produkto.
Dažni pavyzdžiai
- Hidratacija (alkenas → alkoholis): rūgštinė katalizė (H2SO4, H3O+) su karbokationiniu tarpininku. Kartais naudojama hidroboracija‑oksidacija (BH3 → H2O2/NaOH), kuri duoda anti‑Markovnikov esybę ir syn stereocheminį prisijungimą.
- Hidrohalogeninimas (HBr, HCl): elektrofilinė adicija; be peroksidų – Markovnikov produktas, su peroksidais – anti‑Markovnikov (per radikalinį mechanizmą).
- Halogeninimas (Br2, Cl2): vyksta per halonium joną → rezultatas dažniausiai anti‑adicija.
- Hidrogenacija (H2, metalinis katalizatorius: Pd, Pt, Ni): π‑jungtis redukuojama iki viengubo ryšio; prisijungimas dažniausiai vyksta syn būdu.
- Epoksidacija ir atidarymas: alkeno epoksidas (pvz., perrūgštimi) gali būti atidaromas nukleofilais suteikiant diolį arba kitą produktą, stereochemiškai kontroliuotą.
- Diels–Alder reakcija: konjuguotas dienas + dienofilas → ciklinis produktas; concerted mechanizmas, labai stereospecifinis.
- Nukleofilinė adicija prie karbonilo: Grignardo reagentai (R–MgX) ar lithiummetalai prijungia alkilgrupes prie aldehidų/ketonų, formuodami alkoholus po protonavimo; ciano adicija duoda cianohidrinius produktus.
- Michael adicija (1,4‑adacija): nukleofilai prisijungia prie α,β‑nenasybtintų karbonilių sistemų (enonų), svarbi organinei sintezei.
Reakcijos sąlygos, katalizatoriai ir pritaikymas
Adityvinių reakcijų sąlygos priklauso nuo mechanizmo: rūgštinės/protinių katalizės (H+, Lewis rūgštys), metaliniai katalizatoriai (hidrogenacijai, kationinių kompleksų formavimuisi), radikalų iniciatoriai (peroksidai) arba specifiniai reagentai (BH3, perrūgštys, halogenai). Šios reakcijos yra kertinės organinėje sintezėje: jos naudojamos vaistų, agrochemikalų, polimerų ir kompleksinių molekulių gamybai. Pvz., papildymas prie dvigubo ryšio yra esminis žingsnis kuriant funkcionalizuotus angliavandenilio produktus arba sudarant vinilines monomerų grandines adityvine (pridėjimo) polimerizacija.
Praktinės pastabos ir ribotumai
- Adityvinės reakcijos dažnai konkuruoja su izomerizacija arba eliminacija, priklausomai nuo temperatūros, katalizatoriaus ir substrato stabilumo.
- Stereocheminis kontrolės laipsnis gali reikalauti chirališkų katalizatorių arba specialių reagentų (enantioselekyvios adicijos).
- Konjuguotose sistemose būtina apsvarstyti 1,2‑ ir 1,4‑adicijos galimybes – produktas priklausys nuo reagentų pobūdžio ir sąlygų.
Apibendrinant, adityvinė reakcija yra plati kategorija, apimanti įvairius mechanizmus (elektrofilinius, nukleofilinius, radikalinius, pericyklinius) ir lemianti daugumos organinių sintezės žingsnių pasekmių: regiocheminės, stereocheminės ir kinetinės savybės lemia galutinį produktą ir jo pritaikymą.