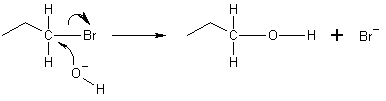
Nukleofilas - tai rūšis, kuri atiduoda elektronų porą elektrofilui, kad reakcijos metu susidarytų cheminis ryšys. Visos molekulės ar jonai, turintys laisvą elektronų porą, gali būti nukleofilai. Ši elektronų pora vadinama vieniša pora. Kadangi nukleofilai atiduoda elektronus, jie atitinka Lewiso bazių apibrėžtį.
Nukleofilinis apibūdina nukleofilo trauką prie branduolių. Nukleofiliškumas, kartais vadinamas nukleofilo stiprumu, reiškia medžiagos nukleofilinį pobūdį ir dažnai naudojamas atomų traukos palyginimui.
Neutralios nukleofilinės reakcijos su tirpikliais, tokiais kaip alkoholiai ir vanduo, vadinamos "solvolize". Nukleofilai gali dalyvauti nukleofilinio pakeitimo reakcijose. Šiose reakcijose nukleofilą pritraukia visiškas arba dalinis teigiamas krūvis.
Savybės ir veiksniai, lemiantys nukleofiliškumą
- Elektrinis krūvis: neigiami jonai (pvz., OH−, Cl−) paprastai yra stipresni nukleofilai nei neutralios dalelės (pvz., H2O), nes turi daugiau laisvų elektronų.
- Elektronegatyvumas: mažesnės elektronegatyvumo atomo prie elektronų poros reiškia didesnį nukleofilinį aktyvumą (pvz., I− dažnai yra labiau nukleofilinis nei F− protiniuose tirpikliuose).
- Poliarizuojamumas (minkštumas): didesni, labiau poliarizuojami atakai (pvz., S−, I−) gerai reaguoja su minkštais elektrofilių centrais. HSAB (hard–soft acid–base) principas padeda prognozuoti sąveikas tarp kietų/minkštų nukleofilų ir elektrofilių.
- Sterinė įtaka: didelis „apgaubimas“ apie atakos centrą mažina nukleofiliškumą (pvz., trietilaminas yra silpnesnis nukleofilas už mažesnes aminogrupes dėl erdvinio užstojimo).
- Tirpiklis: poliniai protiniai tirpikliai (pvz., vanduo, alkoholis) slopina anijonus hidrogeno jungtimis (solvatacija), mažindami jų nukleofiliškumą; poliniai aprotiniai tirpikliai (pvz., DMSO, DMF) sustiprina mažų anionų nukleofiliškumą.
- Rezonavimas ir hibridizacija: delokalizuoti elektronai (pvz., karboksilatai) yra mažiau nukleofiliniai nei lokalizuoti; sp2 hibridizuotas anglies centras paprastai yra mažiau reaguojantis už sp3.
- Bazinė jėga vs. nukleofiliškumas: nors bazinis stiprumas (konjuguotos rūgšties pKa) ir nukleofiliškumas dažnai koreliuoja, tai nėra tas pats: bazė medžiaga siekia protonų, o nukleofilas atakuoja elektrofilius (pvz., F− yra labai bazinis, bet prasčiau nukleofilinis protiniame tirpiklyje nei I−).
Pavyzdžiai
- Anijoniniai nukleofilai: OH−, OR− (alkoksidai), CN−, N3−, halogenidai (Cl−, Br−, I−), HS−, RS−.
- Neitriniai nukleofilai: NH3, R2O (eteriai), H2O, R3P (fosfinai), R2S.
- Specializuoti organometaliniai nukleofilai: Grignardo reagentai (RMgX), organolitio junginiai (RLi), kurie atakuoja elektrofilinius C centrus (pvz., karbonilus) ir sudaro naujus C–C ryšius.
- Karbanionai ir enolatai: labai stiprūs nukleofilai, svarbūs C–C jungimo reakcijose.
Reakcijos, kuriose dalyvauja nukleofilai
- SN2 (vieno žingsnio nukleofilinė substitucija): nukleofilas atakuoja elektrofilinį anglies atomą iš galinės pusės, vyksta apverstas stereocentras; reaguoja geriau esant stipriems nukleofilams ir mažam steriniam užstojimui.
- SN1 (dviejų žingsnių substitucija): pirmiausia susidaro karbokationas, tada nukleofilas prisijungia; nukleofilo stiprumas dažniau neturi didelės įtakos reakcijos greičiui, svarbesnė yra carbokationo stabilizacija.
- Solvolizė: kai tirpiklis pats dalyvauja kaip nukleofilas (pvz., vanduo ar alkoholis užpildo atsiradusį teigiamą centrą), reakcijos kartais vadinamos solvolizėmis (solvolysis).
- Nukleofilinis pridėjimas prie karbonilių: nukleofilai (pvz., R− iš Grignardo reagentų, hidridai iš NaBH4) atakuoja C=O, sudarydami alkoholio funkciją ar naują C–C ryšį.
- Nukleofilinė aromatinė substitucija: kai kuriems aromatiniams žiedams nukleofilai gali prisijungti per pridėjimo–eliminuojimo mechanizmą arba per benzino (benzyne) tarpinius junginius.
Praktinė reikšmė ir patarimai laboratorijoje
- Renkantis nukleofilą sintetinėms reakcijoms, atkreipkite dėmesį ne tik į jo bazinį stiprumą, bet ir į tirpiklio poveikį, sterinį užstojimą ir galimą rezonansinį stabilumą.
- Jei reikia stiprios SN2 reakcijos, naudokite mažai užstotą, neprotinį tirpiklį ir stiprų, gerai tirpų nukleofilą (pvz., CN− DMSO tirpale).
- Norint išvengti pašalinių protonacijų ar solvolizės, kontroliuokite tirpiklio rūšį ir reakcijos sąlygas (temperatūra, koncentracija).
Supratimas apie nukleofilus ir jų savybes yra esminis organinės ir neorganinės chemijos srityse, ypač projektuojant sintezės kelius, prognozuojant reaktyvumą ir pritaikant tinkamas reakcijos sąlygas.