SN 2 reakcija (dar vadinama bimolekuline nukleofiline substitucija) yra organinės chemijos substitucijos reakcija. Tai nukleofilinės pakaitos rūšis, kai nukleofilo vieniša pora atakuoja elektrono trūkumo elektrofilinį centrą ir su juo susijungia, o priešingai orientuota išeinanti grupė — "išeinanti grupe" — vienu žingsniu išstumiamą. Kadangi lėtame, greitį lemiančiame reakcijos etape dalyvauja dvi reaguojančios rūšys (nukleofilas ir substratas), reakcija vadinama bimolekuline nukleofiline substitucija arba SN2.
Mechanizmas
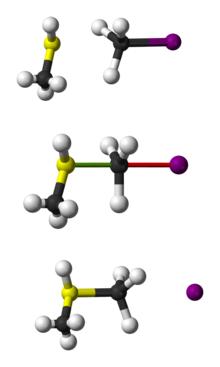
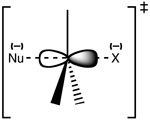
SN2 yra koncertinė (vieno žingsnio) reakcija: nukleofilas atakuoja nuo substrato priešingos pusės (backside attack), susidaro tranzicinis pentakoordinuotas kompleksas (dalinis junginys), ir išeinanti grupė yra išstumta tuo pačiu metu. Dėl tokios atakos dažnai vyksta Waldeno inversija — stereocentras invertuojasi (pvz., iš R į S konfigūraciją).
Greitis ir kinetika
- SN2 reakcijos greitis apibūdinamas įstatymu: rate = k [nukleofilas][substratas]. Todėl greitis priklauso nuo abiejų reaguojančių rūšių koncentracijų.
- Perėjimo būsena yra energetiškai didesnė už reagėntus — reakcijos energijos profilis turi vieną energijos barjerą (vieno etapo mechanizmas).
Faktoriai, lemiantys SN2 reakciją
- Substrato struktūra: steriškai neužstoti centrai skatina SN2. Tipinė tvarka: metilo > pirminis > antrinis. Terciniai alkilai praktiškai nepatiria SN2 dėl sterinio užstojimo.
- Nukleofilas: stiprus, neperprotonuotas nukleofilas (didelis atominis krūvis, maža elektrono delokalizacija) pagreitina SN2. Pavyzdžiui, OH-, RS-, CN- yra geri nukleofilai.
- Išeinanti grupė: geros išeinančios grupės stabilizuoja negatyvų krūvį ir palengvina išstūmimą. Pavyzdžiui, I- > Br- > Cl-; tosilo grupė (OTs) yra dar geresnė išeinanti grupė.
- Tirpiklis: SN2 dažniau vyksta poliariniuose aprotinėse tirpikliuose (pvz., DMSO, DMF, acetonas), nes jie mažiau solvatuoja anijonus ir leidžia nukleofilui būti reaktyvesniam. Poliariniai protiniai tirpikliai (pvz., vanduo, alkoholiai) solvatuoja nukleofilus ir lėtina SN2.
- Temperatūra ir koncentracijos: didesnė temperatūra paprastai pagreitina reakciją; didesnės reaktantų koncentracijos didina greitį pagal kinetikos lygtį.
Stereochemija
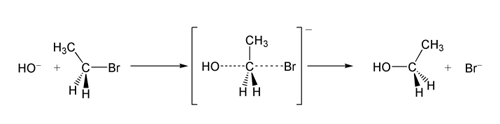
Tipiška SN2 reakcijos savybė – inversija (Waldeno inversija) dėl nukleofilo atakos iš priešingos pusės. Jei substratas turi stereocentrą, produktas paprastai turi priešingą konfigūraciją.
Pavyzdžiai
- Alkilhalidų nukleofilinė pakaita: CH3CH2Br + OH- → CH3CH2OH + Br- (etilo bromidas pakeičiamas hidroksilo grupe).
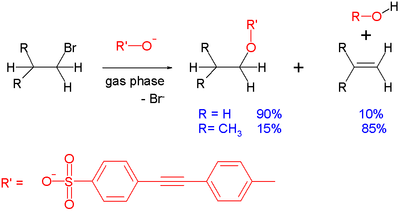
- Williamsono eterio sintezė: R–X + R'O- → R–O–R' + X- (alkilhalidas reaguoja su alkoksidu — klasikinis SN2 pavyzdys, dažnai su pirminiais alkilhalidais).
- Finkelšteino reakcija: R–Cl + NaI (acetone) → R–I + NaCl — halido mainai, vykstantys SN2 mechanizmu (acetonas kaip aprotinis tirpiklis skatina reakciją).
Kitos pastabos ir konkurencija su kitais mechanizmais
- Antriniai centrai gali reaguoti tiek per SN2, tiek per SN1, priklausomai nuo sąlygų (tirpiklis, nukleofilas, temperatūra). Stiprūs baziniai/nukleofilai ir aprotiniai tirpikliai skatina SN2; poliarūs protiniai tirpikliai ir stabilus karbokationas skatina SN1.
- Esant stipriam, steriškai negalimai nukleofilui ir esant β-vietoms vandeniliams, gali vykti E2 eliminacija vietoje pakaitos.
- Svarbu eksperimentiniuose darbo laukuose atsižvelgti į temperatūrą, tirpiklio pasirinkimą ir išeinančios grupės pobūdį, kad būtų pasiektas pageidaujamas mechanizmas ir aukštas selektyvumas.
Apibendrinant: SN2 yra vieno žingsnio, bimolekulinė nukleofilinė substitucija, kuri reikalauja atviros prieigos nukleofilui prie reaktyvaus centro, turi charakteringą stereochimiką (inversiją) ir yra jautri substrato struktūrai, nukleofilui, išeinančiai grupei bei tirpikliui.