Reakcija NS1 yra organinės chemijos pakaitos reakcija, kurioje skilimo ir susidariusio tarpinio produkto savybės lemia reakcijos eigą. „SN“ reiškia nukleofilinį pakeitimą, o „1“ – tai, kad greitį lemiančiame žingsnyje dalyvauja tik viena molekulė (vienmolekulė). Reakcijoje susidaro tarpinis karbokatonas, kuris vėliau reaguoja su nukleofilu.
Mechanizmas — žingsniai ir kinetika
Standartinis NS1 mechanizmas vyksta dviem pagrindiniais etapais:
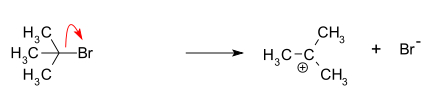
- 1 žingsnis (lėtas, greitį lemiančiasis): išeinantis grupės (pavyzdžiui, halogenido arba protonuota hidroksigrupė) atsiskyrimas nuo substrato ir teigiamo tarpinis karbokatonas susidarymas. Šis žingsnis yra energijos barjeras ir kontroliuoja reakcijos greitį.
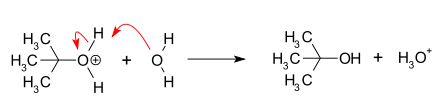
- 2 žingsnis (greitas): nukleofilas prisijungia prie planarinio karbokationo iš bet kurios pusės, sudarydamas galutinį produktą.
Kinetika: reakcijos greitis priklauso tik nuo substrato koncentracijos, taigi greičio išraiška yra rate = k[substratas] – tai atitinka pirmos eilės reakciją.
Stereochemija ir joninė pora
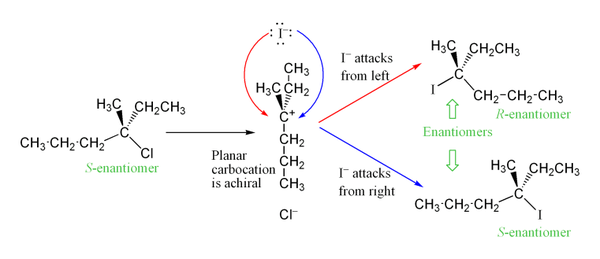
Kadangi tarpinis karbokatonas yra plokščias (sp2 hibridizacija), prisijungimas iš abiejų pusių teoriškai lemia rase-mizaciją (mišinį enantiomerų santykį), kai reaguoja chirališki substratai. Vis dėlto praktikoje dažnai stebima dalinė išsaugojimas arba preferencinė invercija dėl „ioninės poros“ (angl. intimate ion pair) – išeinantis anijonas gali trumpam dengti vieną karbokationo pusę ir nukreipti nukleofilo ataką.
Veiksniai, lemiantys NS1 reakciją
- Substratas: reakcija palankiausia tais atvejais, kai susidaro stabilus karbokationas: tretiniai > antriniai > pirminiai. Stabilumą didina alkilinių grupių izohyperkonjugacija ir rezonansinis delokalizavimas.
- Išeinanti grupė: geros išeinančios grupės (pvz., halogenidai, tos, kurios gali stabiliai palikti kaip anijonai arba protonuotos OH grupės) skatina reakciją.
- Solventas: poliniai protiniai (pvz., etanol, vanduo) tirpikliai gerai stabilizuoja jonus ir skatina NS1 mechanizmą, nes jie mažina karbokationo energiją.
- Nukleofilo stiprumas: skirtingai nei NS2, nukleofilo stiprumas NS1 reakcioje yra mažiau svarbus, nes nukleofilas nedalyvauja greitį lemiančiame žingsnyje.
- Temperatūra ir rūgštinės sąlygos: rūgštinės sąlygos (protonavimas alkoholių) palengvina išeinančios grupės atskilimą; aukštesnė temperatūra dažnai skatina eliminuojančius procesus (E1) konkurencijoje su NS1.
Karbokationo poslinkiai ir šalutiniai procesai
Susidarius karbokationui, gali vykti struktūrinės pertvarkos (pvz., hidridų ar alkilinių perėjimų – hydride arba alkyl shift), jei tai sukuria stabilesnį karbokationą. Tai gali lemti netikėtus produktus arba izomerizaciją. Be to, NS1 dažnai konkuruoja su E1 eliminacija, ypač esant aukštesnei temperatūrai arba silpniems nukleofilams.
Pavyzdžiai ir praktinė reikšmė
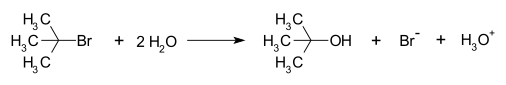
- Tert-butilchlorido hidrolizė: typiškas NS1 pavyzdys — tert-butilo halogenidas atsiskaido, susidaro tert-butilo karbokationas, kuris reaguoja su vandeniu.
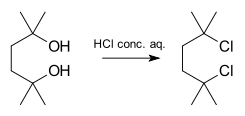
- Antriniai ir tretiniai alkoholių reakcijos rūgštinėmis sąlygomis: protonavus OH grupę ji tampa geresne išeinančia grupe, todėl vyksta NS1 mechanizmas formuojant karbokationą.
- Organinės sintezės planavimas: žinant, ar procesas vyks per NS1 ar NS2, galima pasirinkti tinkamas sąlygas (tirpiklius, temperatūrą, katalizatorių) bei išvengti nepageidaujamų perėjimų ar poslinkių.
Sutrumpinimai ir nomenklatūra
Neorganinės chemijos specialistų tarpe NS1 reakcija dažnai vadinama disociaciniu mechanizmu. Pirmą kartą reakcijos mechanizmą 1940 m. pasiūlė Christopheris Ingoldas ir kt., o nuo tada mechanizmo principai plačiai taikomi tiek akademinėje, tiek pramoninėje organinėje chemijoje.
Santrauka: NS1 pasižymi vienmolekuliniu greitį lemiančiu žingsniu, kuriame susidaro karbokationas. Reakcijos eiga labai priklauso nuo karbokationo stabilumo, išeinančios grupės kokybės ir tirpiklio savybių; ji dažnai konkuruoja su E1 eliminacija, o poslinkiai gali pakeisti galutinį produktą.