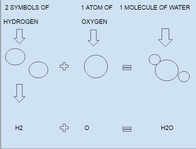
Cheminė formulė - tai būdas, kuriuo chemikai apibūdina molekulę. Formulėje nurodoma, kokie atomai ir kiek jų yra molekulėje. Kartais formulėje nurodoma, kaip atomai yra susiję, o kartais formulėje nurodomas atomų išsidėstymas erdvėje.
Raidė rodo, koks cheminis elementas yra kiekvienas atomas. Indeksas rodo kiekvienos rūšies atomo skaičių. Pavyzdžiui, vandenilio peroksido formulė yra H2O2. Metanas turi vieną anglies (C) atomą ir keturis vandenilio atomus; cheminė formulė yra CH4. Cukraus molekulėje gliukozėje yra šeši anglies, dvylika vandenilio ir šeši deguonies atomai, todėl jos cheminė formulė yra C6H12O6.
Cheminės formulės naudojamos cheminėse lygtyse cheminėms reakcijoms aprašyti.
Šią cheminių formulių rašymo sistemą sukūrė XIX a. švedų chemikas Jonsas Jokūbas Berzelijus.
Tipai ir reikšmė
- Molekulinė formulė nurodo kiekvieno elemento atomų skaičių molekulėje (pvz., H2O, CO2, C6H12O6).
- Empirinė formulė pateikia elementų santykį mažiausiais sveikaisiais skaičiais (pvz., gliukozės empirė formulė yra CH2O, vandenilio peroksido empirinė formulė — HO).
- Struktūrinė (arba išdėstymo) formulė rodo, kaip atomai yra tarpusavyje sujungti (pvz., H–O–H arba CH3CH2OH). Ji gali parodyti ryšius viengubus, dvigubus ar trigubus.
- Sutrumpinta (konsoliduota) struktūrinė formulė (pvz., CH3COOH) yra patogi organinėms molekulėms rašyti.
- Skeleto (skeletal) formulė cheminėje organinėje chemijoje vaizduoja tik anglies grandinę ir funkcines grupes be visų vandenilio atomų (naudinga kompleksinėms molekulėms).
- Stereocheminė formulė perteikia erdvinį atomų išsidėstymą (cis/trans, R/S konfigūracijas).
Rašymo taisyklės ir ženklai
- Elementų simboliai rašomi pagal tarptautinę sistemą (pvz., H, C, O, Na, Cl).
- Skaičius, nurodantys atomų skaičių, rašomi kaip indeksai (subscript): H2O, CO2. Jeigu vieno elemento yra tik vienas, indeksas paprastai nerašomas (pvz., CH4, o ne C1H4).
- Jei vienoje grupėje yra keli tokie pat atomai, naudojami skliaustai: Ca(OH)2 reiškia vieną kalcio ir dvi hidroksido grupes.
- Koeficientai formulėje (priekyje) vartojami cheminėse lygtose reagento ar produkto kiekį nurodyti: 2H2 + O2 → 2H2O. Koeficientas nurodo molekulių skaičių, o indeksai — atomų skaičių vienoje molekulėje.
- Ionei nurodyti naudojami rodikliai (superskriptai): Na+, SO42−. Izotopų žymėjimui viršuje nurodomas masės skaičius: 14C.
- Hidrolius ir kristalizuotas vanduo žymimas tašku: CuSO4·5H2O.
- Fazės būklė cheminėse lygtose rašoma skliaustuose: (s) kietas, (l) skystis, (g) dujos, (aq) vandeninis tirpalas.
- Elementų tvarka formulėje: organinėse junginiuose dažnai vartojama Hill taisyklė (C pirmas, H antras, po to likę elementai alfabetine tvarka). Anorganinėms medžiagoms elementai paprastai rašomi alfabetine tvarka arba pagal tradiciją (pvz., NaCl).
Pavyzdžiai ir paaiškinimai
- Vanduo: H2O — 2 vandenilio ir 1 deguonies atomai, struktūrinis vaizdas H–O–H.
- Anglies dioksidas: CO2 — vienas anglies ir du deguonies atomai, su dvigubais C=O ryšiais.
- Metanas: CH4 — vienas C ir keturi H atomai, tetraedrinė geometrija.
- Vandenilio peroksidas: H2O2 — molekulinė ir empirinė formulės (HO) skiriasi; empirinė rodo santykį, molekulinė — tikrą atomų skaičių.
- Geležies(III) sulfatas: Fe2(SO4)3 — skliaustai reikalingi daugkartinėms poliatominėms grupėms.
- Natriumo jonas: Na+, nitrato anijonas: NO3− — jonų formulė rodo krūvį.
Struktūrinės formulės ir rezonansas
Struktūrinės formulės (pvz., H–O–H arba H–C≡C–H) parodo ryšius. Kai junginyje yra keli įmanomi elektronų išdėstymo variantai, vartojamas rezonansinis vaizdas, kuriame faktinė struktūra yra tarp kelių meso formų (pavyzdžiui, benzenas arba karbonatai).
Kur naudojamos cheminės formulės
Cheminės formulės naudojamos:
- cheminių reakcijų užrašymui ir balansavimui,
- medžiagų savybių identifikavimui,
- stoichiometrijos skaičiavimams (reagento ir produkto kiekiams apskaičiuoti),
- medžiagų klasifikavimui (organinės vs. anorg., joninės vs. kovalentinės).
Naudingos pastabos
- Formulė nenurodo visada erdvinės molekulės geometrijos; tam reikalingi strukturiniai arba stereocheminiai žymėjimai.
- Formulės rašymo taisyklės gali skirtis priklausomai nuo konteksto (paprastos laboratorinės užrašos vs. tarptautiniai nomenklatūros standartai, pvz., IUPAC).
- Istoriškai ši sistema buvo sustyguota ir išpopuliarinta XIX a. pradžioje, kai Jonsas Jokūbas Berzelijus pasiūlė elementų simbolių ir formulių rašymo normas.