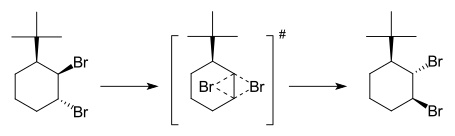
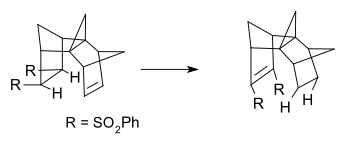
Dytropinė reakcija yra cheminės reakcijos rūšis. Ji vyksta tada, kai organinis junginys pakeičia savo struktūrą. Du pakaitalai peršoka iš vienos molekulės vietos į kitą. Tai periciklinė valentinė izomerizacija, kai du sigma ryšiai vienu metu persikelia į naują vietą toje pačioje molekulėje. Dyotropinės reakcijos yra svarbios organinėje chemijoje. Jomis galima paaiškinti, kaip vyksta tam tikros reakcijos. Dytropinės reakcijos gali būti naudingas žingsnis gaminant dideles ir sudėtingas molekules. Pirmą kartą dytropines reakcijas 1971 m. aprašė Manfredas T. Reetzas. Pavadinimas "dyotropinė reakcija" kilęs iš graikų kalbos žodžio dyo, reiškiančio "du". "Persitvarkymas" reiškia, kad reakcijos metu keičiasi ryšiai tarp vienos molekulės atomų.
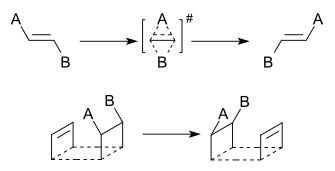
I tipo reakcijos metu dvi migruojančios grupės keičiasi savo santykinėmis padėtimis. II tipo reakcijos metu vyksta migracija į naujas jungčių vietas be apsikeitimo padėtimis.
Mekanizmas — kaip vyksta dytropinis persitvarkymas?
Dytropinė reakcija dažniausiai vyksta koncertiškai per periciklinį perėjimo būsenos kompleksą: tuo pačiu metu verčiami (sruvena) du sigma-ryšiai ir susidaro du nauji ryšiai. Tokia vienu metu vykstanti migracija leidžia išvengti ilgalaikio joninio ar radikalinio tarpinio etapo. Tačiau, priklausomai nuo substituentų, temperatūros ar katalizatorių, gali būti ir kitokios (pvz., stepwise arba radikalinės) alternatyvos — tai nustatoma eksperimentiniais ir skaičiavimų metodais.
Tipai (išplėstinis paaiškinimas)
- I tipo (1,2-dytropiniai) — dvi grupės mainosi vietomis tarp artimų atomų: grupė A pereina į B poziciją, o B — į A poziciją. Tai galima laikyti apsikeitimo procesu.
- II tipo — abi grupės migruoja, bet ne apsikeičia savo vietomis; jos persikelia į naujas atskiras vietas molekulėje (pvz., iš dviejų kaimyninių centrų į du kitus centrus).
Pavyzdžiai ir dažniausi migruojantys fragmentai
Dažniausi dytropinių persitvarkymų pavyzdžiai apima:
- halogenų (pvz., chloro, bromo) migracijas;
- alkilinius ar alkinilinius fragmentus;
- organosilicio (silyl) grupių persikėlimus;
- kitus funkcinius fragmentus, kurie gali stabilizuoti perėjimo būseną.
Konkrečios molekulės pavyzdžiai aptinkami literatūroje: dažnai minimos dvynaudžių halogenų persikėlimo reakcijos ir organosilicio migracijos, kurios naudojamos ir sintetinėje chemijoje.
Stereochemija ir termodinamika
Stereocheminis rezultatas stipriai priklauso nuo reakcijos mechanizmo ir molekulės geometrijos. Koncertiška migracija gali išlaikyti arba pakeisti santykinį stereocentų išdėstymą priklausomai nuo to, ar persikėlimai vyksta suprafacialiai ar antarafacialiai, ir nuo erdvinės prieigos. Termodinamiškai procesas gali būti tiek grįžtamas, tiek negrįžtamas — tai priklauso nuo galutinės struktūros stabilumo ir reakcijos aktyvavimo energetikos.
Praktinė reikšmė ir taikymai
- Dytropinės reakcijos yra naudingos sintetinėje organinėje chemijoje: jos leidžia perkelti funkcines grupes, keisti skeletalinę architektūrą ir pasiekti struktūras, kurios kitaip būtų sudėtingai gaunamos.
- Naudojamos kuriant sudėtingas natūralių produktų struktūras, ingredientus vaistų sintezėje ir medžiagų chemijoje.
- Konceptualiai svarbios suprantant periciklinės ir valentinės izomerizacijos mechanizmus bei jų įtaką cheminėms transformacijoms.
Kaip nustatoma, ar reakcija yra dytropinė?
- Eksperimentai: izotopų žymėjimas ir NMR stebėjimai gali parodyti, kad dvi grupės vienu metu pasikeičia vietomis arba migruoja.
- Struktūriniai metodai: rentgeno struktūros analizė (XRD) gali paliudyti galutinę produktų konfigūraciją.
- Skaičiavimai: kvantinės cheminės skaičiavimo metodikos leidžia modeliuoti perėjimo būsenas ir palyginti koncertiškos bei stepwise alternatyvos energijas.
Trumpai apie istoriją
Manfredas T. Reetz 1971 m. suformulavo ir aprašė šią reakcijų klasę, pateikdamas idėją apie dvigubą, simetrišką arba koordinuotą migraciją toje pačioje molekulėje. Nuo to laiko dyotropiniai procesai buvo tirti tiek eksperimentaliai, tiek teoriniu požiūriu.
Išvados
Dytropinė reakcija — svarbus organinės chemijos mechanistinis ir sintetinės strategijos elementas. Ji leidžia suprasti, kaip kai kurie funkciniai pokyčiai molekulėje gali įvykti vienu koordinuotu žingsniu ir suteikia galimybes planuoti sudėtingas molekulines transformacijas. Norint taikyti dytropinius persitvarkymus praktikoje, būtina atidžiai vertinti molekulės geometriją, substituentų poveikį ir reakcijos sąlygas.