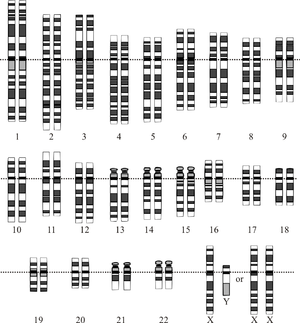
Žmogaus genomas saugomas 23 chromosomų porose, esančiose ląstelės branduolyje ir mažojoje mitochondrijų DNR. Haploidinis žmogaus genomas sudaro maždaug 3,1–3,3 milijardo DNR bazių porų; diploidiniame organizme (kai turime dvi kiekvienos chromosomos kopijas) — apie 6,2–6,6 milijardo bazių porų. Genomas apima tiek baltymų koduojančias sekas (maždaug 20–25 tūkst. genų), tiek dideles nebaigtų kodavimo sričių (vadinamos „ne-koduojančios“ DNR) masyvus: reguliacines sekas, pasikartojančias sekas, intronus, pseudogenus ir įvairius nenustatytos funkcijos elementus.
Pagrindinės sąvokos
- Genas — DNR regionas, kuris gali duoti nurodymus baltymo ar funkciniu RNR formavimuisi.
- Promoteriai ir enhanceriai — reguliacinės sekos, kurios valdo, kada ir kur genai yra aktyvinami.
- Epigenetika — cheminės modifikacijos (pvz., DNR metilinimas, histonų modifikacijos), kurios veikia genų raišką nekeičiant pačios sekos.
- Variacijos — vieno nukleotido polimorfizmai (SNP), struktūrinės variacijos ir didesnės genomo reorganizacijos, kurios lemia tarpindividinę įvairovę ir gali turėti įtakos sveikatai.
Žmogaus genomo projektas (HGP) ir referencinis genomas
Vykdant Žmogaus genomo projektą (HGP) buvo sukurta etaloninė seka, kuri visame pasaulyje naudojama biologijoje ir medicinoje. Nature paskelbė valstybės finansuojamo projekto ataskaitą, o Science paskelbė Celera straipsnį — abu darbai apibendrino pirmąsias žmogaus genomo sekos versijas ir jos analizę. 2003 ir 2005 m. buvo paskelbti patobulinti projektai, kuriais buvo užpildyta iki ≈92 % sekos.
Reikšmingi tolesni patobulinimai (pvz., naujos kartos genomo surinkimo ir žemėlapių versijos, kaip GRCh37 ir GRCh38) sumažino klaidas ir užpildė dalį spragų. Pastaraisiais metais (2021–2022 m.) Tarptautinis telomerų–iki–telomerų (T2T) konsorciumas ir kiti tyrimai papildė ankstesnius etalonus, užpildydami sudėtingas sritis (pvz., centromerines ir kitų pasikartojančių elementų sekas), o tai padėjo sukurti dar išsamesnį žmogaus genomo vaizdą.
Sekos technologijos ir genomo analizė
Žmogaus DNR sekos nustatymas vystėsi nuo Sangerio metodo iki masinės paralelinės analizės (NGS), o vėliau atsirado ilgų skaitymų technologijos (PacBio, Oxford Nanopore). Kiekviena technologija turi privalumų: trumpi skaitymai — didelis tikslumas ir talpa; ilgi skaitymai — gebėjimas išspręsti pasikartojančias, struktūrines regionų problemas ir sujungti haplotipus.
Reikšmingi aspektai:
- Referencinis genomas yra sudarytas iš kelių donorų ir nėra visiškai atvaizduota visų populiacijų įvairovė; todėl dabar kuriami pangenomai (pan-genome), kurie apima daugiau variacijų.
- Individualios sekos (visas genome sekvencijavimas) leidžia nustatyti paveldimas ligas, jautrumą vaistams, rizikos žymenis ir vėžinių ląstelių mutacijas.
Genų reguliacija ir ENCODE
Naujausiame ENCODE projekte tiriama, kaip valdomi genai — identifikuojamos promotorių, enhancerių, transkribuojamų regionų ir kitų reguliacinių elementų vietos ir funkcijos. ENCODE siekia suprasti, kurios DNR dalys aktyviai dalyvauja ląstelės biologijoje (pvz., transkribuojamos ar baltymų pririšimo vietos), tačiau projekto rezultatai sukėlė diskusijų dėl termino „funkcija“ apibrėžties: ar elementas, kuris turi molekulinį ženklą, būtinai turi organisminei reikšmei?
Genų reguliacija yra daugiasluoksnė:
- Transkripcijos faktoriai ir jų pririšimo vietos.
- Chromatino struktūra ir 3D genomo organizacija (pvz., TAD – topologically associating domains), kuri lemia genų ir reguliacinių elementų sąveikas.
- Epigenetiniai žymenys: DNR metilinimas, histonų modifikacijos, kiti baltymų kompleksai.
- Ne-koduojančios RNR (miRNA, lncRNA ir kt.) — reguliuoja transkripciją, transliaciją ir RNR stabilumą.
Praktinės taikymo sritys
- Medicininė genetika: paveldimų ligų diagnostika, genų tyrimas ligoms paaiškinti.
- Onkologija: navikų genomų sekos analizė leidžia rasti gydytinas mutacijas ir stebėti atsparumo mechanizmus.
- Farmakogenomika: vaistų dozavimas ir pasirinkimas pagal paciento genetinį profilį.
- Populiacijų genetika ir genealogija: migracijos, paveldimumo ir rizikos žymenų analizė.
- Tyrimai ir biotechnologijos: genų redagavimas (pvz., CRISPR), modelių kūrimas ir biologinių mechanizmų aiškinimas.
Etiniai, teisiniai ir socialiniai klausimai
Genominė informacija yra labai jautri. Pagrindiniai iššūkiai:
- Privatumas ir duomenų apsauga: kaip saugoti seką ir genetikos duomenis nuo neleistino naudojimo.
- Diskriminacija (draudimo, darbo vietos) dėl genetinių ypatumų.
- Informuotas sutikimas ir sprendimai dėl incidentinių radinių (pvz., atradus ligai reikšmingą mutaciją tyrimo metu).
- Lygiavertis prieinamumas: ar pažangios genomikos paslaugos bus prieinamos visiems, nepriklausomai nuo socioekonominės padėties.
Ateities kryptys
- Pangenomai ir didesnė populiacijų įvairovė referenciniuose duomenyse.
- Vienaląstelis genomas (single-cell) ir erdvinis genomas (spatial genomics) — kaip genai veikia atskirame ląstelių kontekste ir audiniuose.
- Visiškas asmeninis genomų taikymas medicinoje, kartu sprendžiant etinius klausimus ir didinant duomenų saugumą.
- Išsamus funkcinis genomo žemėlapis — kuri DNR dalis ir kada tikrai turi biologinę reikšmę.
Dabar daug žinoma apie DNR sekas, esančias mūsų chromosomose. Dabar iš dalies žinoma, ką iš tikrųjų veikia DNR. Šių žinių taikymas praktikoje dar tik prasideda, tačiau jau keičia diagnostikos ir gydymo galimybes, taip pat kelia naujus mokslinius ir visuomeninius iššūkius.