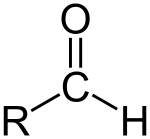
Aldehidas (/ˈæældɪhaɪd/) yra organinis junginys, kuriame yra formilo (arba aldehidinė) grupė. Formilio grupė – tai molekulės dalis, kurios bendroji struktūra yra R-CHO (R žymi šoninę organinę grupę). Ji susideda iš anglies atomų, kurių vienas yra dvigubai susijungęs su deguonimi (C=O), o tas pats anglis dar prisijungęs prie vandenilio ir prie R grupe. Grupė neturinti šoninės grandinės (kai R = H) vadinama aldehidine grupe arba formilo grupe. Aldehidai nuo ketonų skiriasi tuo, kad aldehidų molekulėse formilo grupė yra molekulės gale (anglies atomas prijungtas prie bent vieno vandenilio), o ketonuose karbonilo anglis būna viduryje. Aldehidai yra plačiai paplitę organinėje chemijoje ir daugelyje natūralių bei sintetikos produktų; daugelis kvapiųjų medžiagų yra aldehidai.
Struktūra ir pavadinimas
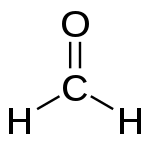
- Standartinė formulė: R–CHO. Jei R = H, gaunamas formaldehidas (metanalas, HCHO).
- Pavadinimai: sisteminėje nomenklatūroje naudojamas galūnė „-al“ (pvz., CH3CHO – etanalis, acetaldehydas).
- Pavyzdžiai: formaldehidas (CH2O), acetaldehidas (CH3CHO), benzaldehidas (C6H5CHO).
Fizinės savybės
- Aldehidai paprastai yra poliarūs junginiai dėl karbonilo grupės; tai lemia didesnį virimo tašką, palyginti su nevandeniliniais angliavandeniliais to paties molinio svorio, bet mažesnį nei atitinkamų alkoholų.
- Mažos molekulės aldehidai (pvz., formaldehidas, acetaldehydas) yra dujinės arba labai lakių skysčių būklės kambario temperatūroje.
- Aldehidinį protoną (–CHO) 1H NMR spektre paprastai matyti ties 9–10 ppm; IR spektre matomas karbonilo pralaidumas ~1720 cm−1 (priklauso nuo konjugacijos ir aplinkos).
Cheminės savybės ir pagrindinės reakcijos
- Elektrofilinis karbonilo anglis: aldehido karbonilas yra stipriai elektrofilinis, todėl lengvai reaguoja su nukleofilais (nukleofilinės adicijos reakcijos). Pavyzdžiui, R–CHO + Nu− → R–C(OH)(Nu).
- Redukcija: aldehidai redukuojami iki pirminių alkoholų (pvz., NaBH4 arba katalizinė vandenilinė redukcija).
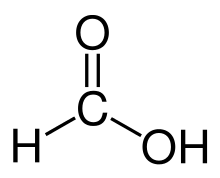
- Oksidacija: aldehidai lengvai oksiduojasi iki atitinkamų riebalinių rūgščių (R–CHO → R–COOH); tai atsitinka ir oro sąlygomis, ir oksidatoriais (KMnO4, K2Cr2O7). Formaldehidas ypač lengvai oksiduojamas.
- Nukleofilinė adicija: formuoja cianohetrinus (reakcija su HCN), hemiacetalus/acetalus (priešais alkoholį ir rūgštingumą), iminus arba Schiffo bazių (su aminais).
- Aldolio kondensacija: aldehidai, turintys α-vandenilio atomus, kondensuojasi bazėje arba rūgštyje į β‑hidroksialdehidus, kurie dehidratuodami duoda α,β‑nenasotinus aldehidus/aromatus junginius.
- Cannizzaro reakcija: neenolizuojami aldehidai (be α‑H) stiprioje bazėje disproporcionuoja – vienas aldehidas redukuojamas į alkoholį, kitas oksiduojamas į karboksilatą (pvz., benzaldehido reakcija).
- Wittig reakcija: aldehidai reaguoja su fosforinio ylide, sudarydami alkenus – dažna metodika organinėje sintezėje.
- Grignard priedas: organometaliniai reagentai (R′MgX) nukleofilškai atakuoja aldehidų karbonilą ir po darbupio (workup) duoda antrinius alkoholus (iš formaldehido gaunami pirminiai alkoholiai).
Gamyba
- Pramonėje formaldehidas gaminamas dehidrogenacijos arba oksidacinio metanolio atskaidymo (metanolio oksidacija per katalizatorių, pvz., sidabrą ar geležies – molibdeno pagrindu).
- Alifatiniai aldehidai dažnai gaunami oksidavus atitinkamus pirminius alkoholus arba naudojant hidroformilinimą (OXO procesą) – alkenuose įvedant CO ir H2 katalizės sąlygomis.
- Laboratorijose aldehidai gali būti gaunami redukuojant rūgštinius chloridus arba oksiduojant alkoholus bei kitais regio- ir chemoselektoriais metodais.
Panaudojimas
- Formalinas ir dervos: formaldehidas – pagrindinė žaliava ureato‑formaldehido ir fenol‑formaldehido dervoms, naudojamoms klijavimui, baldų ir statybinių medžiagų gamyboje.
- Parfumerija ir skonio pramonė: daug aldehidų (pvz., benzaldehidas, citrinalas, cinnamaldehidas) suteikia būdingus aromatus ir naudojami kvapų bei skonio kompozicijose.
- Cheminė sintezė: aldehidai yra universalūs tarpiniai produktai vaistų, agrochemikalų ir kitų sudėtingų molekulių sintezėje (Wittig, Grignard, aldol reakcijos ir kt.).
- Konservantai ir dezinfekantai: formaldehidas naudojamas tam tikrose dezinfekavimo ir konservavimo formulėse (dėl to yra svarbus biologinių mėginių fiksavimo srityje).
Saugumas ir toksikologija
- Formaldehidas yra dirginantis ir pripažintas kancerogenas (IARC grupė 1). Ilgalaikė arba aukšta ekspozicija sukelia kvėpavimo takų, odos ir akies dirginimą; reikia vengti garų įkvėpimo ir odos kontakto.
- Acetaldehidas – toksiškas, dirginantis, taip pat metabolitas alkoholiui; didesnės koncentracijos gali sukelti galvos skausmą, pykinimą ir kt.
- Darbo vietose būtina tinkama ventiliacija, apsauga (pirštinės, akiniai), laikytis saugos duomenų lapų (SDS) ir teisinių ribinių verčių.
Analizė ir atpažinimas
- IR spektrometrijoje matomas stiprus C=O pralaidumas ~1720 cm−1 (pakinta priklausomai nuo konjugacijos).
- 1H NMR: formilo –CHO signalas ~9–10 ppm, leidžia atskirti nuo kitų protonų.
- Chromatografija (GC, HPLC) kartu su derivatizacija (pvz., DNPH – 2,4‑dinitrofenilhidrazinas) dažnai naudojama aldehidų kiekybiniam nustatymui.
Aldehidai yra cheminiai junginiai su dideliu sintezės ir pramoniniu reikšmingumu: jų reaktivumas (lengva nukleofilinė adicija, oksidacija ir kondensacijos reakcijos) suteikia daug galimybių kurti naujas medžiagas ir natūralias bei sintetines kvapų medžiagas. Dėl kai kurių aldehidų toksiškumo ypač svarbu laikytis saugos taisyklių juos naudojant.