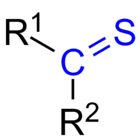
Tioketonas (arba tionas) yra bet kuri molekulė, turinti R2C=S grupę. Tai tarsi ketonas, kuriame deguonies atomas pakeistas sieros atomu. Sieros atomas sudaro dvigubą jungtį su anglies atomu ir turi dvi vienišas poras, todėl C=S ryšys yra gerai polarizuotas (Cδ+–Sδ−) ir cheminėmis savybėmis skiriasi nuo įprasto C=O.
Savybės
Tioketonai pasižymi keliomis specifinėmis savybėmis, kurios lemia jų cheminį elgesį:
- Didelis elektrofilinis pobūdis: anglies atomui prie C=S tenka didesnis teigiamas krūvis nei įprastame karbonile, todėl tioketonai yra stiprūs elektrofilai ir reaguoja su nukleofilais lengviau nei atitinkami ketonai.
- Mažesnė π* energija ir spalvos: pakeitus O → S, π→π* ir n→π* energijos skirtumai mažėja, todėl daugelis tioketonų turi intensyvias spalvas (pvz., tiobenzofenonas yra violetinis).
- Reaktyvumas ir nestabilumas: dauguma paprastų tioketonų yra laki ir cheminiai nestabilūs – linkę polimerizuotis, dimerizuotis arba dalyvauti cikloapjungimo reakcijose. Aromatinės ar steriškai užstotos struktūros suteikia didesnį stabilumą.
- Fizinės savybės: kai kurie tioketonai turi stiprų kvapą; jų C=S ryšys skiriasi IR ir UV–Vis spektre palyginti su karbonilais.
Gautos reakcijos ir cheminis elgesys
Tioketonai elgiasi panašiai į karbonilus, bet kuriamoms reakcijoms būdingas didesnis tempas arba kita reakcijų specifika:
- Nukleofilinės pridėtinės reakcijos: nukleofilai (pvz., aminai, tiolai, vandenilio donorai) prijungia prie anglies C=C=S centro, formuodami atitinkamas pridėtines produktų rūšis. Dėl didesnio elektrofilinio pobūdžio šios reakcijos dažnai vyksta lengviau nei su ketonais.
- Cikloapjungimai: tioketonai dažnai dalyvauja [4+2] (Diels–Alder tipo) ir kitose pericycliniųėjose reakcijose su dienais, taip formuodami heterociklines arba kitas kompleksines struktūras. Jie taip pat gali dimerizuotis per [2+2] ar kitas ciklinimo reakcijas.
- Desulfurizacija ir oksidacija: tioketonai gali būti oksiduojami į atitinkamus ketonus (S → O) arba desulfurizuojami (pvz., Raney Ni) į angliavandenilius/ketonus, priklausomai nuo sąlygų.
- Transformacijos į kitus funkcinius tipus: tioketonai gali būti naudojami kaip pradinės medžiagos heterociklų sintezėje arba garderinių grandinių modifikacijose.
- Stabilesni palyginamieji pavyzdžiai: jei viena iš R grupių yra vandenilis, molekulė yra sieros aldehido (analogas aldehidui). Toks junginys vadinamas tialiu ir yra dar reaktyvesnis už tioketoną dėl dar ryškesnio elektrofilinio centro.
Gaminimo būdai
Dažniausiai taikomos tioketonų sintezės strategijos:
- Karbonilų „thionacija“: įprastas ir patikimas būdas – ketonų arba aldehidų transformacija į tioketonus naudojant reagentus, tokius kaip Lawesson’o reagent arba P4S10 (fosforo pentasulfidas). Šios reakcijos pakeičia C=O funkciją į C=S.
- Tiesioginė konstrukcija: kai kurių tioketonų sintezė vyksta per organometalines tarpininkes ar kondensacijas, priklausomai nuo norimos struktūros.
Spektroskopija ir atpažinimas
Tioketonų C=S grupė suteikia atpažįstamus spektroskopinius požymius:
- UV–Vis: dėl sumažėjusios π* energijos daugeliui tioketonų matomas n→π* pereinamasis ruožas, kas gali lemti intensyvią spalvą.
- IR: C=S ištrūkis ir kiti susiję vibraciniai signalai skiriasi nuo C=O, todėl IR spektras padeda identifikuoti tioketoną (konkrečios bangos ilgio ribos priklauso nuo substituentų).
- NMR: cheminiai poslinkiai protonams ir angliams prie tioketono centro skiriasi nuo įprasto karbonilo analogų, todėl NMR padeda patvirtinti struktūrą.
Stabilumas, sauga ir praktiškos pastabos
Daugelis tioketonų yra reaktyvūs ir, ypač paprastos alkilinės rūšys, gali polimerizuotis arba šildomos suyra. Stabilesni tioketonai yra tie, kurių C atomas steriškai uždengtas arba susietas su aromatiniais žiedais. Dirbant su tioketonais rekomenduojama naudoti inertinę atmosferą (argoną/azotą), žemesnę temperatūrą ir vengti ilgalaikio laikymo esant šilumai ar šviesai. Kai kurie junginiai turi stiprų kvapą ir gali būti toksiški, todėl reikalingos įprastos laboratorinės apsaugos priemonės.
Panaudojimas
Tioketonai yra svarbūs organinės sintezės tarpinių gaminių komponentai: jie naudojami cikloapjungimo reakcijose, heterociklų sintezėje, medžiagų ir dažiklių chemijoje bei kaip reagento komponentai specializuotose transformacijose. Dėl savo didelio elektrofilinio pobūdžio ir poliarumo jie suteikia galimybes formuoti struktūras, kurių ne visada lengva gauti iš įprastų karbonilų.
Apibendrinant: tioketonai yra C=S turintys junginiai, kurie daugeliu atvejų yra labiau reaktyvūs nei jų oksigeniniai analogai. Jie pasižymi specifiniu spektroskopiniu elgesiu, dažnai intensyvia spalva ir plačiu panaudojimu sintezėje, tačiau reikalauja atsargumo dėl stabilumo ir reaktivityvumo.