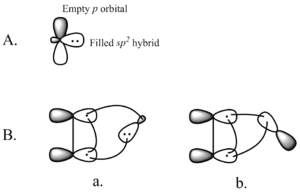
Cheletropinės reakcijos - tai periciklinės reakcijos rūšis, kai vieno iš reagentų atomas įgauna du naujus ryšius. Periciklinė reakcija yra tokia, kai pereinamoji būsena apima ciklinę atomų aibę ir su ja susijusią ciklinę sąveikaujančių orbitalių aibę. Šiame cikliniame masyve vyksta σ ir π ryšių pertvarkymas.
Apibrėžimas ir pagrindinės savybės
Cheletropinės reakcijos yra cikloadjunkcijos poklasis. Joms būdinga, kad viename iš reagentų abu nauji ryšiai sudaromi su tuo pačiu atomu arba atvirkščiai – du ryšiai iš karto nutrūksta tame pačiame atome. Tai atskiria cheletropines reakcijas nuo įprastų cikloadjunkcijų, kur nauji ryšiai susidaro tarp skirtingų atomų. Reakcija gali vykti tiek kaip cheletropinė adicija (maža molekulė prijungiama prie daugiauženkliu junginio), tiek kaip cheletropinė ekstruzija (išmetama maža, stabili molekulė).
Mechanizmas ir orbitalinė simetrija
Cheletropinės reakcijos dažniausiai yra koncertinės (vieno žingsnio) periciklinės reakcijos, kurių pereinamojoje būsenoje dalyvauja uždaras orbitalių ratas. Woodward–Hoffmann taisyklės (konservacija orbitalių simetrijos) lemia, ar konkreti cheletropinė reakcija yra leidžiama termo- arba fotoindukuotomis sąlygomis. Svarbus aspektas yra tai, ar mažas reagentas – pvz., SO2 arba karbenas – reaguoja suprafacial ar antarafacial būdu santykyje su π-sistemos orbitalėmis.
Singletiniai ir tripletiniai karbenai: dauguma cheletropinių adicijų su karbenais vyksta singletinių karbenų atveju kaip koncertinės reakcijos, o tripletiniai karbenai dažnai reaguoja per laisvųjų radikalų tarpininkus (žingsniškai), todėl stereochemija ir kinetika skiriasi.
Pavyzdžiai
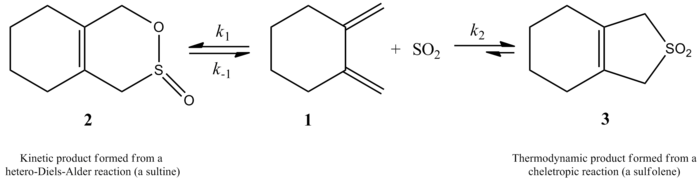
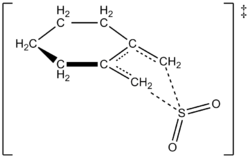
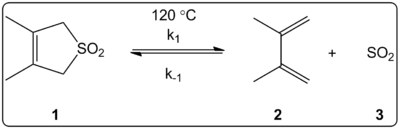
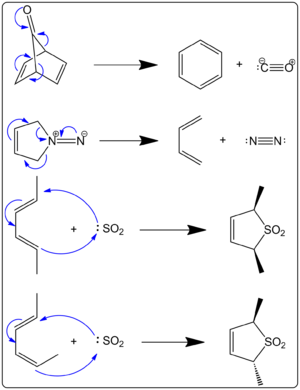
- SO2 + 1,3-butadienas → sulfolenas: tai klasikinis cheletropinės adicijos pavyzdys, kurio metu sieros atomas SO2 užmezga du ryšius su butadieno galais ir susidaro ciklinis sulfono darinys (sulfolenas). Reakcija reversyvi – sulfolenas termiškai gali išskirti SO2 (cheletropinė ekstruzija), atkurdamas butadieną.
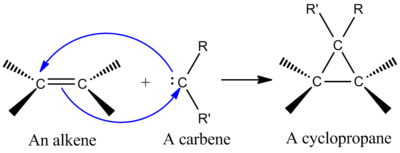
- Karbenų adicija prie alkenų: singletiniai karbenai (pvz., dichlorokarbenas) prijungia karbeno anglies atomą prie dvigubo ryšio, sudarydami ciklopropano žiedą. Abu nauji ryšiai formuojami prie to pačio karbeno atomo, todėl tai laikoma cheletropine adicija.
- Cheletropinės ekstruzijos: termiškai arba fotochemiškai vykstančiose reakcijose gali išsiskirti maži stabilūs dujiniai produktai, tokie kaip CO arba N2, kas suteikia didelį entropinį postūmį reakcijai. Pavyzdžiui, daug organinių perėjimų ir terminio skaidymo reakcijų pasižymi CO arba N2 išsiskyrimu kaip varomąja jėga.
Termodinaminiai ir kinetiniai veiksniai
Cheletropinių reakcijų vyksmą lemia keletas veiksnių:
- Orbitalinė sąveika: suderinamumas tarp dalyvaujančių orbitalių (π ir tinkamų σ arba n orbitalių) yra itin svarbus.
- Elektroniniai efektai: elektroną atitraukiančios ar donorinės grupės daugiaženklyje gali stabilizuoti arba destabilizuoti pereinamąją būseną.
- Temperatūra ir entropija: cheletropinės ekstruzijos, kuriomis išsiskiria dujos (pvz., CO arba N2), dažnai yra entropiškai skatinamos ir geriau vyksta aukštesnėje temperatūroje.
- Katalizatoriai ir terpė: Lewis rūgštys ar metaliniai katalizatoriai gali suaktyvinti tam tikras π-sistemas arba stabilizuoti perinamas būsenas, keičiant reakcijos greitį ir selektyvumą.
Stereochemija ir selektyvumas
Nors daug cheletropinių adicijų yra koncertinės ir todėl stereospecifiškos, galutinė stereochemija priklauso nuo reagentų pobūdžio (pvz., singlet vs triplet karbenas), reagento priėjimo kampo ir izoliuotų tarpininkų nebuvimo. Woodward–Hoffmann principai leidžia prognozuoti, ar tam tikra konfigūracija yra orbitalių požiūriu leidžiama termiškai ar fotochemškai.
Praktinė reikšmė
Cheletropinės reakcijos yra vertingos sintezės chemijoje:
- jos leidžia efektyviai įvesti mažus heteroatomų vienetus (pvz., SO2, karbenai) į didesnius karkasus,
- ekstruzijos reakcijos naudojamos kaip būdas generuoti reaguojančias tarpinės būsenas arba išlaisvinti dujas, kurios paskatina tolimesnes transformacijas,
- supratimas apie orbitalinę simetriją padeda projektuoti selektyvias ir stereospecifines sintezes.
Santrauka: cheletropinės reakcijos yra specialus periciklinių procesų atvejis, kuriuose vienas atomas sudaro arba nutraukia du ryšius tuo pačiu metu. Jos gali vykti kaip adicijos arba ekstruzijos ir jų eiga stipriai priklauso nuo orbitalių simetrijos, reagentų tipo (pvz., singlet/triplet karbenai) bei termodinamikos ir kinetikos veiksnių. Daug praktinių sintezės problemų sprendžiamos pasitelkiant cheletropines transformacijas.

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)