Fermentai - tai ląstelėse esančios baltymų molekulės, kurios veikia kaip biologiniai katalizatoriai. Fermentai pagreitina chemines reakcijas organizme, bet jų metu nesunaudojami, todėl gali būti naudojami vėl ir vėl. Fermentai sumažina aktyvacijos energiją, leidžiant reakcijoms vykti žymiai greičiau ir prie mažesnių temperatūrų nei be fermentų.
Beveik visoms gyvų organizmų biocheminėms reakcijoms reikia fermentų. Naudojant fermentą cheminės reakcijos vyksta daug greičiau, nei vyktų be fermento.p39 Kiti biokatalizatoriai yra katalizuojančios RNR molekulės, vadinamos ribozimais.
Reakcijos pradžioje esančios medžiagos vadinamos substratais. Reakcijos pabaigoje esančios medžiagos yra produktai. Fermentai veikia substratus ir paverčia juos produktais. Fermentų tyrimas vadinamas enzimologija.
Pirmąjį fermentą 1833 m. rado Anselmas Payenas. Jis išskyrė medžiagą, pavadintą diastaze (šiandien dažnai vadinama amilaze), kuri skaidė krakmolą.
Fermentų sandara ir veikimo mechanizmas
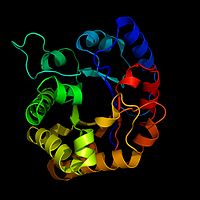
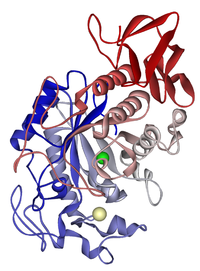
Fermentai dažniausiai yra baltymai, sudaryti iš ilgos aminorūgščių grandinės, kuri sulenkiama į specifinę trimatę struktūrą. Svarbiausia struktūrinė vieta yra aktyvusis centras — mažas vietos ruožas fermento, kuriame substratas prisijungia ir kur vyksta cheminė reakcija. Aktiviųjų centrų forma ir cheminės savybės užtikrina fermentų specifiškumą: vienas fermentas dažnai veikia tik vieną arba nedidelį kelių panašių substratų rinkinį.
Veikimo modeliai:
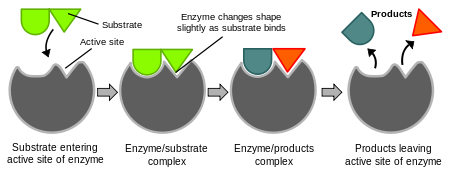
- „Lock and key“ (spyna ir raktas) — substratas tikslingai įsiterpia į aktyvųjį centrą.
- „Induced fit“ (sukeltas prisitaikymas) — prisijungus substratui fermentas šiek tiek keičia formą, kad geriau apglėbtų substratą ir paskatintų reakciją.
Fermentų klasifikacija
Pasaulyje plačiai naudojama fermentų klasifikacija pagal tarptautinę EC (Enzyme Commission) sistemą, kuri skirsto fermentus į šešias pagrindines klases:
- Oxidoreduktazės — dalyvauja oksidacijai ir redukcijai.
- Transferazės — perkeliančios chemines grupes tarp molekulių.
- Hydrolazės — suskaidančios ryšius per hidrolizę (pvz., proteazės, amilazės).
- Lyazės — šalina grupes be hidrolizės, formuoja dvigubas jungtis.
- Izomerazės — keičiančios molekulės izomerinę struktūrą.
- Ligazės (syntetazės) — sujungiančios dvi molekules, dažnai naudojant ATP energiją.
Kofaktorai ir kofermentai
Fermentų kinetika ir reguliavimas
Fermentų aktyvumas dažnai aprašomas Michaeliso–Menten kinetika, kur svarbūs parametrai yra Vmax (maksimalus reakcijos greitis) ir Km (substrato koncentracija, prie kurios reakcijos greitis siekia pusę Vmax). Šie parametrai atspindi fermento efektyvumą ir afinitetą substratui.
Fermentų veikla reguliuojama įvairiais būdais:
- Allosterinė regulacija — molekulės prisijungimas prie neaktyvaus centro keičia fermento aktyvumą.
- Kovalentinės modifikacijos — pvz., fosforilinimas/dezfosforilinimas aktyvuoja arba slopina fermentus.
- Atgalinė inhibicija (feedback inhibition) — galutinio produkto kaupimasis slopina ankstesnį biosintezės žingsnį.
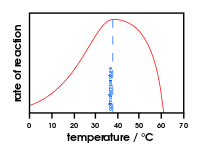
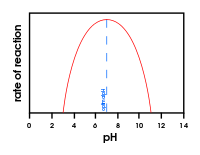
- Besikeičiantys aplinkos veiksniai — temperatūra, pH, joninė jėga ir substrato koncentracija stipriai veikia fermentų aktyvumą.
Inhibitorių tipai
Fermentai gali būti slopinami su skirtingais mechanizmais:
- Konkurencinis inhibitorius — varžosi su substratu dėl prisijungimo prie aktyviojo centro.
- Nekonkurencinis inhibitorius — prisijungia kitur ir mažina fermento aktyvumą nepriklausomai nuo substrato koncentracijos.
- Nepalankus/nergrįžtamas slopinimas — inhibitorius kovalentiškai pakeičia fermentą (pvz., acetilcholino esterazės slopinimas organofosfatais).
Biologinė, medicininė ir pramoninė reikšmė
Fermentai yra gyvybiškai svarbūs: jie kontroliuoja metabolinius kelius, energijos gamybą (pvz., ATP sintezė), DNR replikaciją ir remontą (pvz., DNR polimerazės), baltymų virsmą (proteazės), virškinimą (pvz., pepsinas, amilazė, lipazė) ir daugelį kitų procesų.
Medicinoje fermentų trūkumai sukelia ligas — pavyzdžiui, laktazės trūkumas sukelia laktozės netoleravimą, o tam tikrų metabolinių fermentų trūkumai sukelia paveldimas sutrikimus (pvz., fenilketonurija dėl fenilalanino hidroksilazės nepakankamumo). Fermentai taip pat naudojami kaip diagnostiniai žymenys (pvz., kepenų fermentai, širdies fermentai kraujyje).
Pramonėje fermentai plačiai naudojami: maisto pramonėje (pieno fermentai, sūrio gamyba), skalbimo priemonėse (proteazės ir lipazės pašalina dėmes), biotechnologijose (rekombinantinių fermentų gamyba), farmacijoje (enziminiai diagnostiniai testai) ir ekologinėje technologijoje (biodegradacija ir bioremediacija).
Enzimologijos tyrimai ir matavimai
Fermentų aktyvumas matuojamas specialiais testais (enziminėmis analizėmis). Dažnai naudojami parametrai: aktyvumo vienetai (IU), Vmax ir Km. Taip pat naudojami metodai struktūrai tirti — rentgeno kristalografija, NMR ir kryo-elektroninė mikroskopija.
Naudingi pavyzdžiai
- Amilazė — skaido krakmolą į cukrus.
- Pepsinas ir tripsinas — skaido baltymus virškinimo trakte.
- ATP sintazė — sintezuoja ATP ląstelėje.
- DNR polimerazė — daugina genetinę medžiagą replikacijos metu.
- Laktazė — skaido laktozę; jos nepakankamumas sukelia laktozės netoleravimą.
Apibendrinant, fermentai yra specializuoti baltymai, esminiai gyvybiniams procesams ir plačiai pritaikomi medicinoje bei pramonėje. Jų savybės — specifika, greitis ir reguliacija — leidžia gyviems organizmams tiksliai valdyti cheminių reakcijų tinklus.