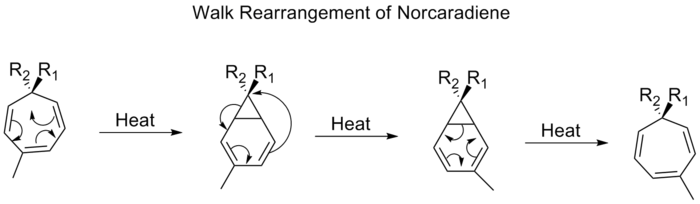
Organinėje chemijoje sigmatropinė reakcija yra periciklinė reakcija, kurios metu vienas σ ryšys „persikelia“ iš vienos vietos molekulėje į kitą, o tuo pačiu persitvarko susijusi π elektronų sistema. Sigmatropinėje reakcijoje paprastai nedalyvauja išoriniai katalizatoriai — tai intramolekulinus, nekatalizuojamus persitvarkymai — tačiau kai kuriuos variantus gali pagreitinti Lewiso rūgštis ar pereinamųjų metalų kompleksai. Pavadinimas kilo sujungus „sigma“ (viengubos anglies–anglies jungtys) ir graikų žodį tropos (posūkis). Tai klasikinė persitvarkymo reakcija: atomai nepalieka molekulės ir naujų atomų neatsiranda, bet ryšiai persiskirsto, o substitutas gali pajudėti iš vienos π jungčių sistemos dalies į kitą.
Tipai ir žymėjimas
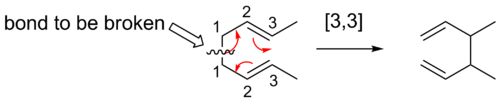
Sigmatropinės pertvarkos žymimos kaip [i,j], kur i ir j reiškia atstumą (atitinkamai iš kairės ir dešinės pusės) nuo migruojančio σ ryšio iki naujos σ jungties susidarymo vietos per π sistemą. Tipiški pavyzdžiai yra [3,3] (Cope'o ir Claisen tipo), [1,5] (dažnai vandenilio perslinkimai) ir [2,3] arba [3,2] pertvarkymai (pvz., 2,3-Wittig ar sulfoxidų perstūmimai).
Mechanizmas ir orbitalinė simetrija
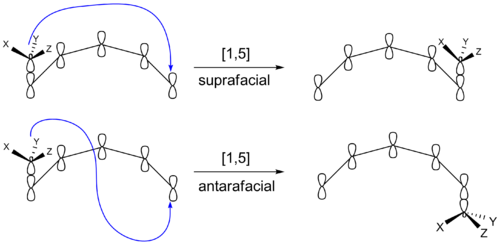
Sigmatropinės reakcijos dažniausiai vyksta per vieną koordinuotą, ciklinį pereinamosios būsenos etapą — tai yra koncertinis mechanizmas. Reakcijos lemiamas veiksnys yra orbitalių simetrija. Pagal Woodward–Hoffmann taisykles leidžiamumas nustatomas pagal dalyvaujančių π elektronų skaičių ir tai, ar perslinkimas vyksta suprafacial (vienos molekulės paviršiaus pusėje) ar antarafacial (per skirtingas molekulės puses) būdu.
- Therminės (šilumos) sigmatropinės reak. paprastai leidžiamos, kai pereinančiojo ciklo orbitalių simetrija atitinka Hückel tipo sąlygas (pvz., daugeliui 6 elektr. [3,3] ir [1,5] hidridų perslinkimų būdingas suprafacial veikimas).
- Fotocheminės sąlygos gali pakeisti leidžiamumą: reakcijos, kurios termiškai yra „uždraustos“, dažnai vyksta apšvitinus, nes excitacija keičia orbitalių užpildymą.
Stereochemija ir migracijos pobūdis
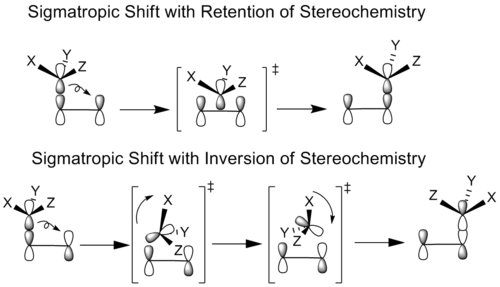
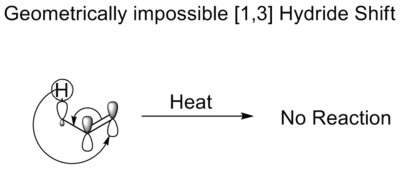
Sigmatropiniai perstūmimai gali išlaikyti arba inverstuoti stereocheminę informaciją, priklausomai nuo perslinkimo topologijos (suprafacial arba antarafacial). Pvz., suprafacialus vandenilio perstūmimas dažnai reiškia stereocheminį išsaugojimą (retention) dėl to, kad hidrogenas migruoja per tą pačią molekulės pusę. Antaarafacialūs perstūmimai reikalauja geometriškai sudėtingesnio perėjimo ir kartais nėra įmanomi dėl konformacinių apribojimų.
Tipiniai pavyzdžiai
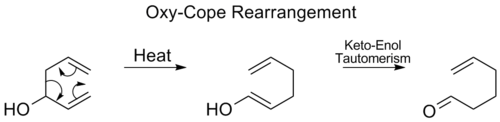
- [3,3] Cope'o pertvarkymas — izomerizacija 1,5-dienų, vykstanti per šešių elektronų ciklinę pereinamąją būseną; dažnai taikoma angliavandenilių skeletonų perstatymui.
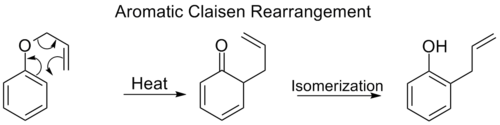
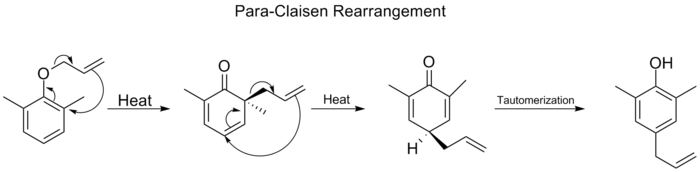
- Claisen pertvarkymas — [3,3] sigmatropinė perestroika, kurioje allyl vinil eteriai arba jų dariniai pereina į karbonilius ar allyl substituotas produktus; itin svarbus sintezėje dėl stereocheminio valdymo.
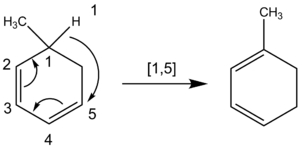
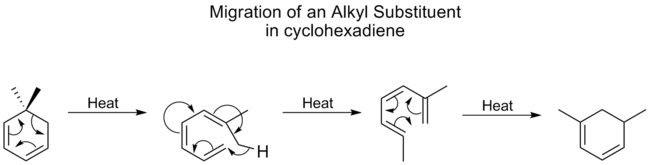
- [1,5] hidridų perstūmimai — dažni termiškai leidžiami perstūmimai, svarbūs izomerizacijose ir alkilų perstumimuose.
- [2,3] ir [3,2] perstūmimai — pvz., 2,3-Wittig ar Mislow–Evans tipų sulfoxidų perstūmimai, kurie naudojami chiralinės informacijos pernešimui.
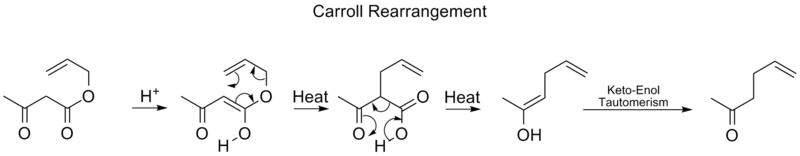
- Carrollo (Carroll) pertvarkymas — dažnai interpretuojamas kaip [3,3] tipo pertvarkymas, kartais lydimas decarboxylation etapų; naudojamas tam tikrų allyl esterių transformacijose.
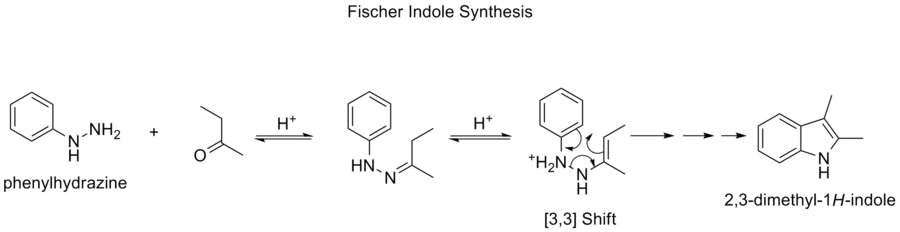
- Fischerio indolo sintezė — tradiciškai minima tarp žinomų procesų, kuriuose atsiranda sigmatropiniai žingsniai (reakcijos sekos metu vyksta perstūmimų ir elektrokliniai etapai).
Katalizė ir alternatyvūs mechanizmai
Nors daug sigmatropinių reakcijų yra nekatalizuotos, egzistuoja modifikacijos, kuriose dalyvauja katalizatoriai:
- Lewiso rūgšties koordinacija prie π sistemos sumažina aktyvacijos energiją ir gali nukreipti reakciją per daugiau poliarinius ar ioninius pereinamuosius etapus.
- Pereinamieji metalai (pvz., Pd, Rh) gali sudaryti tarpininkaujančius kompleksus arba metallaciklus, kuriuose „migruojantis“ fragmentas perkeliamas žingsniais (stepwise), o ne per grynai koncertinį perėjimą.
- Tokių katalizuotų variantų mechanizmas dažnai būna skirtas nuo klasikinio periciklinio modelio ir gali suteikti naują chemiją bei stereochemijos kontrolę.
Analizė ir praktinės taikybė
Sigmatropinės pertvarkos yra plačiai naudojamos sintetinėje organizinėje chemijoje skeletonų rekonstrukcijai, stereocheminiam manipuliavimui ir natūralių produktų sintezei. Mechanistinės išvados gaunamos naudojant izotopinius žymėjimus, kinetikos tyrimus, spektroskopiją ir skaičiavimus. Dėl savo dažnai mažo aktyvavimo barjero ir galimybės vykdyti be ekvivalento reagentų, sigmatropinės reakcijos yra vertingos žygdarbiuose, leidžiančiuose atlikti atomui-evoliucinius pokyčius be atomų praradimo.
Praktiniai pastebėjimai
- Molekulės konformacija ir įtemptumas dažnai lemia, ar tam tikras antarafacial perstūmimas yra įmanomas; dauguma paprastų ciklinių sistemų linkusios vykdyti suprafacialius perstūmimus.
- Substituentų elektroniniai ir steriniai efektai gali reikšmingai pakeisti reakcijos greitį ir selektyvumą.
- Kai kurios reakcijos, kurios grynai pericikliškai yra lėtos arba „uždraustos“, gali būti pagreitintos ar leistinos naudojant fotochemiją arba katalizę.
Apibendrinant, sigmatropinės reakcijos yra fundamentali periciklinė klasė organinės chemijos, kuri leidžia perstatyti ryšius ir atnaujinti molekulinius skeletonus be atomų praradimo — svarbi tiek mechanistinei, tiek taikomosios chemijos praktikai.

![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)


![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)